По данным Университета Джонса Хопкинса, пандемия COVID-19 охватила 188 стран, а по данным L. Yang, D. Tian, W. Liu (2020) – 212 с общим числом заразившихся коронавирусом, превысившим 16,4 млн чел. Количество жертв коронавируса во всем мире превышает 600 тыс. чел. [5]. I. Madabhavi, M. Sarkar, N. Kadakol (2020) обозначили пандемию как катастрофу мировой значимости [6]. Только в России число случаев заражения коронавирусом достигло 818 120, число заболевающих ежедневно превысило 5 600 случаев. В глобальном масштабе наблюдается нарастание скорости распространения коронавируса и ухудшение клинических показателей у пациентов. Несмотря на миллиардное финансирование исследований SARS COV-2, на современном этапе не изучены механизмы повреждения органов дыхания, печени и почек, а также не установлены причины изменений белой пульпы селезенки. Особенно опасно инфицирование для больных, имеющих тяжелые сопутствующие заболевания, в том числе онкологические [7]. Наличие двух штаммов SARS-CoV-2, отличающихся по своей активности в организме при COVID-19, а также 5 геномов, зарегистрированных в базе данных GenBank, свидетельствуют о трудностях на пути создания вакцины против данной вирусной инфекции. S. Kannan, Ali P. Shaik Syed, A. Sheeza, K. Hemalatha (2020) утверждают, что, хотя несколько животных предположительно являются резервуаром для COVID-19, резервуар для животных еще не подтвержден [8]. Анализ 160 образцов генома SARS-CoV-2, выделенных у заболевших людей, позволил установить, что разновидности коронавируса A и C распространены у европейцев и американцев, а в Восточной Азии наиболее распространена разновидность B. Противоречивыми являются данные о продолжительности иммунитета к вирусу SARS-CoV-2. Отсутствует этиотропное и патогенетически обоснованное лечение, заключающееся на современном этапе в симптоматических мероприятиях. Бесполезность применения ИВЛ в качестве реанимационных мероприятий также показала, что повреждение альвеолоцитов является следствием, а не причиной запуска каскада патологических реакций при COVID-19. Неизвестность в вопросе происхождения SARS-CoV-2, спекуляции о преднамеренной генной инженерии SARS-CoV-2 также не способствуют разработке эффективной стратегии в лечении пациентов с COVID-19, как и мер профилактики инфекции. Учитывая скорость распространения заболевания, тяжесть течения, наличие групп риска, составляющих большую часть населения земного шара, решение вопросов патогенеза COVID-19 является на современном этапе наиболее актуальным. Каждый отдельный случай должен быть проанализирован, учтены все особенности течения и исхода заболевания на фоне сопутствующей патологии каждого пациента с COVID-19, чтобы в дальнейшем иметь фундаментальные основы для разработки эффективной стратегии профилактики, лечения и реабилитации пациентов, перенесших инфекцию. Реальные представления о полном ущербе, наносимом организму SARS-CoV-2, на современном этапе отсутствуют. Данные, полученные при анализе материала, взятого при вскрытиях, позволят решить вопрос, насколько в действительности опасна коронавирусная инфекция и ее последствия для организма человека. Обобщение небольшого количества данных о COVID-19 F. Jiang, L. Deng, L. Zhang, Y. Cai, C.W. Cheung, Z. Xia (2020) и наличие относительно минимального количества систематических исследований на основании результатов вскрытия умерших от COVID-19 в начале пандемии связано с опозданием данных о том, что вирус поражает не только легкие, но также иммунную систему и другие органы [9]. В настоящее время не хватает патоморфологических данных о новой коронавирусной полиорганной недостаточности.
Материалы и методы исследования
В работе проведён анализ и обсуждение результатов собственных исследований биоптатов 11 пациентов, умерших от COVID-19, вызванной SARS-CoV-2, с подтверждением PCR. Морфологический метод исследования заключался в изготовлении срезов из парафиновых блоков биоптатов органов жертв SARS-CoV-2 с последующей окраской гематоксилином и эозином в соответствии с классическим протоколом. Анализ препаратов и изготовление иллюстраций выполнены с помощью микроскопа Olympus Bx52 и цифровой камеры DP25.
Результаты исследования и их обсуждение
Клиническая характеристика и распределение материала по возрасту, полу, сопутствующей патологии и морфологическим проявлениям в тканях органов представлены в таблице.
Распределение материала
|
№ /пол |
Возрастные группы |
Контроль |
Сопутствующая патология |
Материал |
||||
|
Печень |
Лёгкие |
Почки |
||||||
|
Ожирение/СD |
Анемия |
ССС патология |
||||||
|
1. ж |
26 лет |
3 |
Анемия неуточненного генеза, Hb 65 г/л Эр. 2,23*1012 |
Атеросклероз аорты в стадии липоидоза |
Гепатит |
Двусторонняя субтотальная пневмония |
Нефрит |
|
|
2. ж |
39 лет |
Язвы желудка и кишечника |
Анемия, эр. 2.12* 1012 Hb 78 г/л |
Атеросклероз аорты в стадии липоидоза, фрагментация кардиомиоцитов |
Гепатолиенальная Т-клеточная лимфома IV Б стадии |
Двусторонняя субтотальная пневмония с десквамативным компонентом в стадии организации, отек легких |
Паренхиматозная дистрофия |
|
|
3. м |
41 год |
Миокардит |
Лимфо-гистоцитарный гепатит |
Тотальная двусторонняя пневмония, острый респираторный дистресс-синдром: гиалиновые мембраны в ткани легких. |
Гнойный нефрит, сепсис, инфаркт |
|||
|
4. ж |
53 года |
Лимфо-гистиоцитарный миокардит |
Паренхиматозная дистрофия |
Двусторонняя тотальная пневмония с десквамативным компонентом, гиалиновые мембраны |
Паренхиматозная дистрофия, очаговый некротический нефроз |
|||
|
5. ж |
61 год |
ГБ, гипертрофия левого желудочка (16 мм), атеросклероз аорты, коронарных и мозговых артерий в стадии липосклероза, атероматоза и кальциноза |
Паренхиматозная дистрофия |
Двусторонняя интерстициальная пневмония с десквамативным компонентом, стазы и сладжи крови в микрососудах легких, диапедезные микрокровоизлияния, отек легких и мозга, диапедезные интраальвеолярные кровоизлияния, эмфизема и дистелектазы легких |
Паренхиматозная дистрофия, почечная недостаточность, мочевина 51,1 ммоль/л; креатинин в моче 153,3 мкмоль/л |
|||
|
6. м |
64 года |
Общее ожирение I–II степени |
Атеросклероз аорты, коронарных артерий в стадии атероматоза и атерокальциноза, гипертоническая болезнь, гипертрофия миокарда (толщина 16 мм), диффузный мелкоочаговый кардиосклероз |
Паренхиматозная дистрофия |
Двусторонняя тотальная пневмония с десквамативным компонентом, гиалиновые мембраны, отек легких |
Паренхиматозная дистрофия Некротический нефроз |
||
|
7. м |
64 года |
Общее ожирение II–III степени |
Атеросклероз аорты, коронарных и почечных артерий в стадии атероматоза и атерокальциноза, гипертоническая болезнь, гипертрофия миокарда (толщина 16 мм), диффузный мелкоочаговый кардиосклероз |
Паренхиматозная дистрофия |
Двусторонняя тотальная пневмония с десквамативным компонентом, гиалиновые мембраны, отек легких |
Паренхиматозная дистрофия |
||
|
Окончание таблицы |
||||||||
|
№ /пол |
Возрастные группы |
Контроль |
Сопутствующая патология |
Материал |
||||
|
Печень |
Лёгкие |
Почки |
||||||
|
Ожирение/СD |
Анемия |
ССС патология |
||||||
|
8. ж |
71 год |
Общее ожирение II степени, СД |
Атеросклероз аорты, коронарных и почечных артерий в стадии атероматоза и атерокальциноза, гипертоническая болезнь, гипертрофия миокарда (толщина 15 мм) |
Паренхиматозная дистрофия |
Двусторонняя субтотальная пневмония с десквамативным компонентом, гиалиновые мембраны, отек легких |
Паренхиматозная дистрофия Некротический нефроз |
||
|
9. м |
71 год |
Фрагментация кардиомиоцитов. Атеросклероз аорты, коронарных артерий в стадии липосклероза и атерокальциноза. ГБ, гипертрофия левого желудочка 15 мм. |
Паренхиматозная дистрофия |
Двусторонняя субтотальная пневмония с десквамативным компонентом в стадии организации, диффузный пневмофиброз, отек легких, карнификация легких, очаговая плоскоклеточная метаплазия альвеолярного эпителия, эмфизема и дистелектазы легких, гиалиновые тромбы, стазы и сладжи крови в микрососудах легких, диапедезные интраальвеолярные кровоизлияния |
паренхиматозная дистрофия, очаговый некротический нефроз |
|||
|
10. м |
74 года |
Общее ожирение II степени, СД |
Атеросклероз аорты, коронарных артерий в стадии липосклероза и атерокальциноза.Гипертоническая болезнь, гипертрофия левого желудочка 15 мм |
Жировая дистрофия печени |
Двусторонняя субтотальная пневмония с десквамативным компонентом, острый респираторный дистресс-синдром: стазы и сладжи крови в микрососудах легких, диапедезные интраальвеолярные кровоизлияния, гиалиновые мембраны, эмфизема и дистелектазы легких. Отек легких |
Некротический нефроз |
||
|
11. ж |
85 лет |
СД |
Анемия, эр. 2.62 *1012 , Hb76 г/л |
Приобретенный субкомпенсированный комбинированный порок сердца: дегенеративный аортальный стеноз с недостаточностью, кардиомегалия (масса 430 г), гипертрофия левого (20 мм) и правого (15 мм) желудочков ГБ, постинфарктный кардиосклероз в задней стенке л. желудочка |
Паренхиматозная дистрофия |
Двусторонняя интерстициальная пневмония с десквамативным компонентом, пневмофиброз, рассеянный гемосидероз. Эмфизема и спайки в плевральной полости справа |
Почечная недостаточность, паренхиматозная дистрофия ретенционные кисты креатинин до 524,7 мкмоль/л |
|
|
ИТОГО 11 6ж/5м |
4/3 |
3 |
11 |
11 |
11 |
11 |
||
Анализ данных пациентов, умерших от COVID-19, показал, что все заболевшие имели патологические изменения в печени, почках и легких; у четырех было ожирение, у трех – сахарный диабет (СД), все (100 %) пациенты имели поражение кровеносных сосудов, а у девяти и ранее наблюдалось повышенное артериальное давление и заболевания коронарных сосудов, в отличие от данных J.S. Rico-Mesa, A. White, A.S. Anderson (2020), указавших, что сердечно-сосудистая патология среди пациентов Уханя выявлена только в 12 % случаев [10]. В наших исследованиях часто отмечались атеросклероз аорты и многоочаговое острое повреждение миоцитов сердца, гипертрофия левого желудочка с толщиной от 15 до 16 мм, кардиосклероз, в одном случае наблюдалась кардиомегалия с массой сердца 430 г, а также фрагментация кардиомиоцитов. Лимфоцитарный миокардит был зарегистрирован у одного пациента. Морфологические особенности острой пневмонии при COVID-19 у пациентов имели в части случаев характерные признаки острой интерстициальной пневмонии с диффузным альвеолярным повреждением, в сочетании с микрососудистым поражением с внутри- и внесосудистым отложением фибрина, а также с образованием микротромбов в артериолах. В мелких сосудах наблюдались гиперплазия эндотелиоцитов, утолщение стенки сосуда, стенозы просветов и окклюзия. Крупные легочные тромбоэмболии с легочными инфарктами и кровоизлияниями отмечены у шести из одиннадцати пациентов. Также имелись множественные двусторонние сегментарные легочные тромбоэмболии с инфарктами и кровоизлияниями, в сочетании с характерной интерстициальной лимфоцитарной пневмонией с интраальвеолярными отложениями фибрина и отсутствием гиалиновых мембран, возможно, представляющих форму перехода к острой фибринозной и организующей пневмонии. Также были отмечены двусторонняя интерстициальная пневмония, субтотальная и тотальная пневмония, соответственно у двух, пяти и четырех пациентов, которые характеризовались десквамативным компонентом, пневмофиброзом, рассеянным гемосидерозом, а также гранулами гемосидерина в цитоплазме макрофагов (рис. 1).
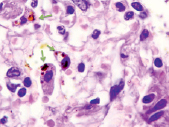
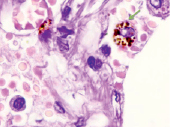
а) б)
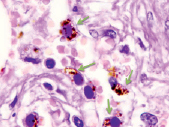
в)
Рис. 1. Легочная интерстициальная гистопатологическая биопсия пациентов с COVID-19: а) 41 год, б) 53 года, в) 74 года. Стрелками зелёного цвета указаны макрофаги с гранулами гемосидерина. Окраска гематоксилином и эозином. Микрофото. Ув. х400
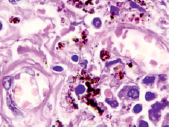
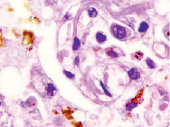
а) б)
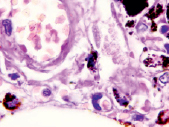
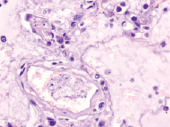
в) г)
Рис. 2. Легочная интерстициальная гистопатологическая биопсия пациентов с COVID-19: а) 64 года, б) 71 год, в) 74 года, г) 85 лет. Стенки сосудов утолщены, эндотелий отсутствует, гипертрофированы перициты. Указаны макрофаги с гранулами гемосидерина. Окраска гематоксилином и эозином. Микрофото. Ув. х400
Также в поле зрения определялись сосуды с гипоплазией эндотелия, гипертрофией эндотелия и перицитов в расщеплениях утолщенной мембраны (рис. 2).
В некоторых исследованиях наблюдались эмфизема и спайки в плевральной полости. Также нами установлено, что на срезах биоптатов легких, печени, почек во всех случаях при летальных исходах в результате заражения SARS-CoV-2 присутствуют патологические изменения всех структур, составляющих гематотканевые барьеры, ведущие к полиорганной недостаточности. Патоморфологические изменения у погибших от COVID-19 лиц молодого возраста (26 и 39 лет), а также пациентки старшей возрастной группы (85 лет) имеют особенности, связанные с анемией. В дополнение к серьезной легочной патологии, в трех случаях нами было обнаружено многоочаговое острое повреждение кардиомиоцитов без воспалительных клеточных инфильтратов, истощение белой пульпы селезенки, очаговая гепатоцеллюлярная дегенерация и клубочковый капиллярный тромбоз. Наличие сердечно-сосудистой патологии было также отмечено L.M. Buja, D.A. Wolf, B. Zhao с соавторами (2020) [11]. 4 пациента страдали ожирением и СД. Кроме того, у некоторых пациентов с COVID-19 также были выявлены неврологические признаки, такие как головная боль, тошнота и рвота. В целом результаты вскрытия подтверждают концепцию, согласно которой патогенез COVID-19 включает повреждение нескольких органов, включая сердце и легкие.
Заключение
Полученные данные подтверждают, что COVID-19 является системным заболеванием с обширным поражением не только легких и сердца, но и всех систем органов. L. Zhang, Y. Jiang, M. Wei, B.H. Cheng, X.C. Zhou, J. Li, J.H. Tian, L. Dong, R.H. Hu (2020) не установили инфицирования новорожденных от беременных женщин с COVID-19 [12]. По мнению Y.C. Li, W.Z. Bai, T.J. Hashikawa (2020), Y. Wu, X. Xu, Z. Chen, J. Duan, K. Hashimoto, L. Yang, C. Liu, C. Yang (2020), все больше доказательств того, что коронавирусы не всегда ограничиваются поражением только дыхательного тракта и что они также могут поражать центральную нервную систему, вызывая неврологические заболевания [13, 14]. Сообщалось об инфицировании мозга вирусами SARS-COV-2 при тяжёлых формах COVID-19, как пациентов, так и экспериментальных животных, при этом ствол мозга был наиболее сильно инфицирован [15]. Кроме того, было продемонстрировано, что некоторые коронавирусы могут распространяться через синапс-связанный путь к медуллярному кардиореспираторному центру от механорецепторов и хеморецепторов в легких и нижних дыхательных путях.
По данным B. Shanmugaraj, K. Siriwattananon, K. Wangkanont, W. Phoolcharoen (2020), некоторые клинические, генетические и эпидемиологические особенности SARS – COVID-19 напоминают инфекцию SARS-CoV, которая после десятилетнего исследования коронавируса по-прежнему не имеет лицензированных вакцин или эффективных терапевтических средств для лечения коронавирусной инфекции, что подчеркивает настоятельную необходимость разработки эффективных вакцин или постконтактной профилактики для предотвращения будущих эпидемий [16]. Следовательно, достижения в области лечения SARS-CoV могут помочь научному сообществу в быстром понимании патогенеза этого вируса и разработать эффективные терапевтические / профилактические средства для лечения и профилактики этой инфекции. Исследование китайских ученых Y. Wang, Y. Wang, Y. Chen, Q. Qin (2019) показало, что большинство пациентов (80,9 %) считаются бессимптомными или имеют легкую форму пневмонии, но опасны тем, что выделяют большое количество вирусов на ранней стадии инфекции, что создает огромные проблемы для сдерживания распространения COVID-19 [17]. Это свидетельствует о необходимости интенсивных исследований SARS-CoV-2 для решения вопросов патогенных механизмов и эпидемиологических характерных особенностей, а также для определения потенциальных лекарственных мишеней, которые будут способствовать разработке эффективных стратегий профилактики и лечения.
Библиографическая ссылка
Рева И.В., Ямамото Т., Гордзиевская К.В., Рассказова М.Е., Вершинина С.С., Фисенко А.Ю., Коцюрбий Е.А., Тудаков В.С., Цегольник Е.С., Усов В.В., Олексенко О.М., Коробкин А.И., Слабенко Э.В., Шиндина А.Д., Рева Г.В. ПАТОГЕНЕЗ КОРОНАВИРУСНОЙ БОЛЕЗНИ 2019 (COVID-19), ВЫЗВАННОЙ SEVERE АCUTE RESPIRATORY SYNDROME CORONAVIRUS (SARS COV-2) // Международный журнал прикладных и фундаментальных исследований. 2020. № 9. С. 23-29;URL: https://applied-research.ru/ru/article/view?id=13122 (дата обращения: 16.05.2026).
DOI: https://doi.org/10.17513/mjpfi.13122

