Введение
В последние годы проводится большое количество исследований полисахаридов и их производных для возможности их применения в качестве наночастиц в системе доставки лекарственных средств. Полисахариды обладают широким разнообразием структуры и свойств из-за их широкого спектра молекулярного веса и химического состава. Полисахариды могут быть легко изменены химически и биохимически. Наличие различных реакционных групп в их структуре (гидроксильных, карбоксильных, аминных) обусловливает повышение их биоадгезии с биологическими тканями, образование нековалентных связей, которые могут быть полезными в улучшении биодоступности препаратов, включённых в систему доставки лекарственных средств [1].
Одним из важных полисахаридов для медицинского применения является пектин. Пектин имеет гетерогенную химическую структуру, основанную на большом количестве поли-D-галактуроновой кислоты, связанной через α(1→4) гликозидными связями. Этот природный полимер имеет от нескольких сотен до около одной тысячи блоков на молекулу, со средней молекулярной массой от 50000 до 180000 Да.
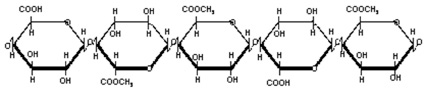
Рис. 1. Схематическое изображение формулы пектина
Вначале пектин применялся в основном в пищевой промышленности как желирующий агент, а в последнее время все чаще применяется в качестве наполнителя в биомедицинских целях [2].
Пектин содержит большое количество поли-D-галактуроновой кислоты, связанной через α-(1→4)-гликозидные связи, где карбоксильные группы находятся частично в метилированной форме (рис. 1).
Пектиновые вещества – природные полисахариды, образованные остатками частично метоксилированной D-галактуроновой кислоты, в которой атом водорода заменен на метоксогруппу (-ОСН3), и по степени метоксилирования подразделяются на высоко- и низкометоксилированные пектины.
Высокометоксилированные пектины образуют высокоэластичные гели за счет изменения сил электростатического отталкивания молекул в кислой среде в присутствии дегидратирующих средств (сахар, кислота). Для таких гелей характерно возвращение формы в исходное состояние после ее изменения при механическом сдвиге.
Низкометоксилированные пектины образуют гели независимо от рН среды и содержания сухих веществ, они образуют студень только в присутствии ионов кальция. Молекулы пектина взаимодействуют между собой за счет карбоксильных групп, связываемых ионами кальция в прочный каркас, удерживающий достаточно жидкости. Эти студни называют ионосвязанными. Температура их гелеобразования повышается с увеличением концентрации ионов кальция. Низкометоксилированные пектины в зависимости от концентрации ионов кальция могут давать различные по консистенции гели – от высоковязких (не восстанавливающих исходную норму после деформирования) до высокоэластичных.
Пектин экстрагируется из свекловичного жома, яблок и цитрусовых корок, природных и доступных углеводов. Пектин богат карбоксильными группами, которые могут привлечь катионы металлов из-за их отрицательного заряда. Эти функциональные группы были описаны как основные группы, участвующие в процессе сорбции металлов.
Множество исследований направлено на получение и изучение свойств производных пектина [3]. Пектаты различных металлов имеют свои характерные свойства. А пектовая кислота, получаемая при окислении эфирных связей, имеет высокую реакционную способность, особенно при связывании металлов за счет образовавшихся карбоксильных групп [4]. Были исследованы кальциевые соли пектовой кислоты, которые сохраняют растворимость и устойчивость пектиновых препаратов в кислых средах. Пектат кальция является потенциальным носителем лекарственных средств в различных формах, например: микросферы, пленки, гели или капельки. Пектат кальция обладает противоязвенным, антимикробным, антимутагенным и противоопухолевым действием, стимулирует работу иммунной системы, выводит токсины из организма, усиливает перистальтику кишечника. Кроме того, пектаты стабилизируют перекисное окисление липидов, активизируют систему естественных антиоксидантов организма, корректируют холестериновый и углеводный обмен.
Целью исследования является получение комплексов пектата кальция из свекловичного пектина, характеристика их состава и структуры, а также определение размера частиц и значения дзета-потенциала.
Материалы и методы исследования
Для получения комплексов пектата кальция были использованы пектиновые вещества, выделенные из свекловичного жома.
Пектин (Пек) был выделен из свекловичного жома.
Получение пектовой кислоты (ПК). 10 г свекловичного пектина растворяют в 1 л 0,1 М NaOH и оставляют на 24 часа. Для извлечения пектовой кислоты раствор обрабатывается изопропиловым спиртом в соотношении 1:1. Осажденная пектовая кислота остается на ночь для стабилизации. Осадок отфильтровывают и последовательно промывают 2-3 раза изопропиловым спиртом и сушат на воздухе. Для получения наноразмерных фракций пектовая кислота (0,1% концентрации, рН 4,0) была обработана ультразвуковыми волнами при интенсивности 1000 кГц в течение 15 минут.
Получение комплексов пектата кальция (PecCa). Для изготовления пектата кальция 2 г пектовой кислоты было растворено в воде при 60 °C при энергичном перемешивании в течение 30 минут. Затем в каждую колбу было добавлено по 10, 20, 30, 40 и 50 мл 0,5% CaCl2 соответственно и воды до 150 мл. Концентрация CaCl2 составляла 0,03, 0,06, 0,09, 0,12 и 0,15% соответственно в каждой колбе. Названия образцов обозначались как Pec-Ca(0.03), Pec-Ca(0.06), и т.д.
Инфракрасные спектры Фурье (FTIR) были получены путем прессования образцов РесА с KBr в таблетки и анализа с помощью спектрометра «ФУРЬЕ ИК-200» (Specod M-80) в спектральном диапазоне 500-4000 см-1.
Размеры частиц определяли методом сканирующей микроскопии.
Дзета-потенциал определялся из ультразвуковых спектров поглощения на DT-1200 электроакустическом спектрометре, DispersionTechnologyInc. Частотный диапазон измерения составлял 1-100 МГц.
Результаты исследования и их обсуждение
Выход конечного продукта с использованием разработанной схемы составил 32%. Конечный продукт – порошок кремового цвета, мелкодисперсный, с остаточной влажностью 8±2%; содержание пектина составляет 74±5%. Характеристики полученных пектина и пектовой кислоты приведены в таблице 1.
Как показано в таблице 1, содержание метоксильных групп снизилось с 3.96 (Пек) до 0,21% (ПК), количество – COOH групп – от 11,39 (Пек) до 17,74% (ПК).
ИК-спектры Фурье пектина и пектовой кислоты весьма схожи по внешнему виду (рис. 2), в высокочастотной области наблюдается широкая полоса поглощения с максимумом при 3420 см-1 и плечом при 3330 см-1, характерная для валентных колебаний гидроксильных групп, участвующих в водородных связях.
Таблица 1
Физико-химический анализ пектиновых веществ
|
Образец |
Практика, % |
Теория, % |
COOH, % |
OCH3, % |
Количество, г |
Выход, % |
||||
|
C |
H |
Зола |
C |
H |
Металл |
|||||
|
Пектин |
40.27 |
6.31 |
2.04 |
42.62 |
4.92 |
- |
11.39 |
3.96 |
- |
- |
|
Пектовая кислота |
38.32 |
5.51 |
0.9 |
40.91 |
4.55 |
- |
17.74 |
0.21 |
11.50 |
80 |
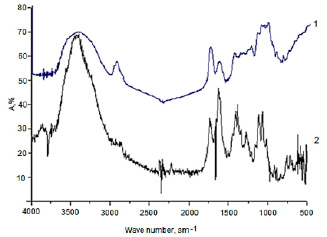
Рис. 2. ИК-спектры Фурье Пек (1) и ПК (2)
В низкочастотной области ν(С=О) полосы 1750 cm-1 при 1730 см-1 проявляется поглощение воды, на которое накладывается асимметричное колебание ионизированных карбоксильных групп νas(COO-) при 1630 см-1. Полоса с максимумом при 1420 см-1 связана с симметричными валентными колебаниями той же группы νs(COO-). Слабое поглощение при 955 см-1 обусловлено колебаниями возмущённого водородной связью гидроксила кольца γ (OH).
Карбоксильная группа является типичной для пектиновых веществ [5]. Спектры пектовой кислоты характеризуются более интенсивными полосами поглощения карбоксильных групп.
Влияние количества кальция на средний размер и дзета-потенциал пектиновых веществ
Пектиновые вещества с высоким содержанием карбоксильных групп взаимодействуют с ионами кальция. Свободные карбоксильные группы распределены в молекуле пектовой кислоты по структурным блокам, поэтому возможно гелеобразование (рис. 3), получающееся при хелатировании ионов кальция остатками карбоксильных и гидроксильных групп в электроотрицательных полостях пектовой кислоты [6].
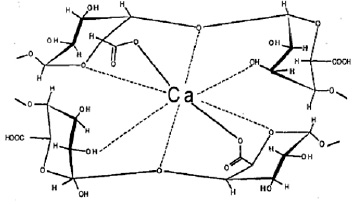
Рис. 3. Структурный фрагмент пектата кальция
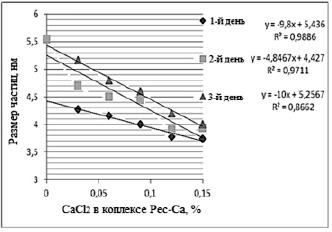
Рис. 4. Средний размер частиц в образцах пектата кальция
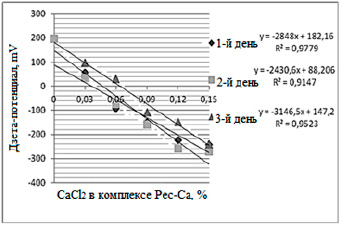
Рис. 5. Дзета-потенциал образцов пектата кальция
Таблица 2
Средний размер, дзета-потенциал и динамическая мобильность образцов пектата кальция
|
Образец |
Средний размер, нм |
ξ, mV |
Динамическая мобильность |
|
1-й день |
|||
|
Pec-Pec |
83,16 |
93104,6 |
0,67 |
|
Рес-Рес-Са(0,03) |
4,28 |
56,58 |
0,07 |
|
Рес-Рес-Са(0,06) |
4,15 |
-92,58 |
0,13 |
|
Рес-Рес-Са(0,09) |
2,7 |
-2887,11 |
0,24 |
|
Рес-Рес-Са(0,12) |
3,78 |
-224,88 |
0,3 |
|
Рес-Рес-Са(0,15) |
3,74 |
-241,86 |
0,38 |
|
2-й день |
|||
|
Pec-Pec |
5,55 |
195,76 |
0,22 |
|
Рес-Рес-Са(0,03) |
4,7 |
34,7 |
0,4 |
|
Рес-Рес-Са(0,06) |
3,4 |
-73,3 |
0,12 |
|
Рес-Рес-Са(0,09) |
4,45 |
-159,8 |
0,24 |
|
Рес-Рес-Са(0,12) |
3,9 |
-258,07 |
0,38 |
|
Рес-Рес-Са(0,15) |
3,94 |
-272,05 |
0,04 |
|
3-й день |
|||
|
Pec-Pec |
90,89 |
3394,6 |
0,26 |
|
Рес-Рес-Са(0,03) |
5,17 |
96,93 |
0,11 |
|
Рес-Рес-Са(0,06) |
4,24 |
30,53 |
0,07 |
|
Рес-Рес-Са(0,09) |
4,4 |
-108,27 |
0,14 |
|
Рес-Рес-Са(0,12) |
6,06 |
-3526,8 |
0,28 |
|
Рес-Рес-Са(0,15) |
6,9 |
-299,36 |
0,3 |
Формирование геля пектата кальция уменьшает растворимость пектовой кислоты. Кальций образует перекрестные связи между двумя молекулами пектовой кислоты в секторе цепи, которая свободна от метоксильных групп. Увеличение содержания хлорида кальция в растворе от 0,03% до 0,15% при комплексообразовании вызывает снижение среднего размера и дзета-потенциала образцов пектата кальция (табл. 2, рис. 4-5). При этом наблюдается повышение степени сшивки и агрегации первоначальных структурных единиц, что вызывает усиление прочности геля и медленное увеличение размеров частиц. Прочность геля возрастает до критической концентрации кальция в системе. Выше этой концентрации прочность геля ослабляется, что обусловлено формированием неоднородной матрицы геля.
Сравнение физических свойств образцов пектина и его комплексов с различным содержанием хлорида кальция приводится в таблице 2.
Заключение
Изменяя содержание кальция в образцах на основе пектовой кислоты, при хранении растворов в течение 2-3 дней, можно изменить средний размер и дзета-потенциал препаратов. Результаты этого исследования позволяют утверждать, что комплексообразование пектовой кислоты с кальцием представляет весьма интересный способ получения препаратов с контролируемым размером частиц.
Библиографическая ссылка
Серикова Л.В., Худайбергенова Э.М., Жоробекова Ш.Ж. ВЛИЯНИЕ СОДЕРЖАНИЯ КАЛЬЦИЯ НА РАЗМЕР ЧАСТИЦ И ДЗЕТА-ПОТЕНЦИАЛ ПЕКТИНОВЫХ ВЕЩЕСТВ // Международный журнал прикладных и фундаментальных исследований. 2024. № 7. С. 30-35;URL: https://applied-research.ru/ru/article/view?id=13645 (дата обращения: 23.03.2026).
DOI: https://doi.org/10.17513/mjpfi.13645

