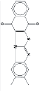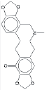Введение
Маклейя сердцевидная (Macleaya cordata (Willd.) R. Br.) и маклейя мелкоплодная (Macleaya microcarpa (Maxim.) Fedde) сем. маковые – Papaveraceae являются источниками изохинолиновых алкалоидов, обладающих важными фармакологическими свойствами – седативным, психотропным, обезболивающим, противомикробным и противовоспалительным действием. Лекарственное растительное сырье (ЛРС) маклейи используется для получения препарата Сангвиритрина – суммы бисульфатов бензо[c]фенантридиновых алкалоидов сангвинарина и хелеритрина, обладающих противомикробным действием [1, 2].
В надземной части маклейи среди алкалоидов превалируют сангвинарин и хелеретрин, сумма которых составляет в листьях образцов растений, выращенных в России (ВИЛАР), до 2,01 %; в листьях M. cordata из Польши – 3,1 и 5,6 мг/г, в траве – 0,7 и 1,8 сангвинарина и хелеритрина соответственно. Также содержатся алкалоиды протопинового типа среди которых превалируют протопин (до 35 %) и аллокриптопин (до 15 %), которые характеризуются выраженным противовоспалительным действием. В образцах листьев M. cordata протопина найдено 1,76 мг/г, в траве – 0,47 мг/г [3–5]. Протопина гидрохлорид, изохинолиновый алкалоид, является специфическим обратимым и конкурентным ингибитором ацетилхолинэстеразы, проявляет противовоспалительную, антимикробную, антиангиогенную, нейропротективную и противоопухолевую активность [3, 6, 7].
Скрининг биологически активных веществ, их качественное и количественное определение требует использования высокоселективных физико-химических методов. Для анализа алкалоидных соединений маклейи используются различные хроматографические методы. ВЭЖХ – квадрупольная времяпролетная масс-спектрометрия чаще всего используется для комплексных исследований сырья и лекарственных средств растительного происхождения. С помощью метода высокоэффективной жидкостной хроматографии (ВЭЖХ) с тандемным масс-селективным детектированием в экстракте маклейи сердцевидной были идентифицированы 32 алкалоида, в том числе 16 минорных алкалоидных соединений, включая нандазурин, гидроксихелидонин, капауридин, (-)-дицентрин, лептопин, адлумидин, такатонин и др. [8, 9].
Протопин также может быть идентифицирован и количественно определен методами газо-жидкостной хромато-масс-спектрометрии (ГЖХ-МС) и тонкослойной хроматографией в комбинации с ГЖХ-МС (ТСХ/ГЖХ-МС). По сравнению с высокоэффективной жидкостной хроматографией в сочетании с масс-спектрометрией (ВЭЖХ-МС) или высокоэффективной жидкостной хроматографией, соединенной с методом ядерного магнитного резонанса (ВЭЖХ-ЯМР), ТСХ/ГХ-МС имеет преимущества в виде короткого времени анализа, низкой стоимости разделения и простоты определения. ТСХ/ГХ-МС больше подходит для быстрого скрининга большого количества образцов небольшой массы из растений, содержащих алкалоиды [10]. Для анализа алкалоидов в экстрактах применялся также биоавтографический анализ ТСХ, совместно с препаративной ТСХ и ГХ-МС [11].
С помощью метода ВЭЖХ выявлено, что доминирующим алкалоидом маклейи сердцевидной, культивируемой в Чехии, является аллокриптопин (3,8–13,6 и 24,2–48,9 мг/г соответственно для надземной и подземной частей). Также присутствовали хелеритрин (2,9–5,7 и 3,6–10,7 мг/г соответственно для надземной и подземной частей), сангвинарин ( 2,9–4,3 и 2,9–10,1 мг/г) и протопин (1,1–5,1 и 0,8–5,8 мг/г для надземной и подземной частей соответственно [5]. Методом ВЭЖХ-МС идентифицированы альфа-аллокриптопин и β-аллокриптопин в плодах M. cordata. В плодах M. cordata и M. microcarpa родом из Китая обнаружены хелидонин, криптонин, ваиллатин, 2-диметилмкрамин, гуннеманнин, корикавидин, мурамин, корикавамин, 2,3-диметилэритопин [2, 12].
Определение алкалоидного состава также проводится с помощью других методов инструментального тестирования, таких как газовая хроматография-масс-спектрометрия (ГХ-МС), капиллярный электрофорез-масс-спектрометрия и ВЭЖХ-ядерный магнитный резонанс (ЯМР). Для разделения и анализа изохинолиновых алкалоидов (протопин, криптопин, синактин, стилопин, бикукуллин, адлюмин, парфумин, фумарилин, фумарофицин, фумаритин, дигидрофумарилин, парфумидин и дигидросангвинарин) успешно применяется метод ГЖХ-МС с использованием хромато-масс-спектрометра Hewlett Packard 5988A MS – HP 5980 GC, оснащенного капиллярной колонкой HP-1 (12 м × 0,2 мм; толщина пленки 0,33 м). Температурная программа колонки: 200 °C в течение 0,8 мин, увеличение со скоростью 10 °C/мин до 250 °C, затем 250 °C в течение 24 мин. Алкалоиды извлекали из ЛРС последовательно экстракцией метанолом, затем выпариванием растворителя, растворением полученного остатка в кислоте хлористоводородной 2,5 %, фильтрацией и подщелачиванием до pH 8 концентрированным аммиаком, экстракцией дихлорметаном [13]. Протопин количествено определяли методом ТСХ с денситометрией и спектрофотометрии в системе растворителей толуол – хлороформ-метанол – 25 % аммиак (5:3:1:1) и циклогексан – диэтиламин (9:1) [14].
Изохинолиновые алкалоиды протопин, криптопин, синактин, стилопин, бикукуллин, адлюмин, парфумин, фумарилин, фумарофицин, фумаритин, дигидрофумарилин, парфумидин и дигидросангвинарин были определены и идентифицированы методом газовой хроматографии-масс-спектрометрии в видах Fumaria и Sarcocapnos [15, 16].
Цель исследования – качественное обнаружение протопина в траве Macleaya cordata и Macleaya microcarpa методом ГЖХ-МС.
Материалы и методы исследования
Объектом исследования служили образцы травы M. cordata и M. microcarpa, выращенных на опытных полях Средне-Волжского филиала ФГБНУ ВИЛАР в 2023 г.
Подготовка пробы: около 1 г (точная навеска) сырья, измельченного до размера частиц, проходящих сквозь сито с отверстиями размером 7 мм, помещают в коническую колбу со шлифом объемом 150 мл, прибавляют 50 мл 70 % спирта, присоединяют к обратному холодильнику и нагревают на кипящей водяной бане в течение 1 ч. Затем колбу охлаждают до комнатной температуры, полученное извлечение фильтруют в колбу объемом 50 мл через бумажный складчатый фильтр.
Анализ проводили методом ГЖХ-МС на хромато-масс-спектрометре 450GC-220MS (Varian, США) с масс-анализатором типа «ионная ловушка». Хроматографическое разделение компонентов пробы проводили на кварцевой капиллярной колонке FactorFOUR VF-5ms (30 м × 0,25 мм). Газ-носитель – гелий с постоянной скоростью потока 1,0 мл/мин. В инжектор хроматографа при температуре 200 °С (деление потока 5) вводят по 1 мкл пробы. Температурная программа колонки: 150 °С – 1 мин, нагрев до 240 °С – 10 °С/мин, изотерма при 240 °С – 30 мин. Включение ионизации на 4-й мин. Общее время анализа – 40 мин.
Идентификацию разделенных компонентов проводили с использованием библиотеки масс-спектров (NIST-08 MS Library and MS Search Program, Version 2f) и алгоритмов сравнения программного обеспечения Saturn (Varian). Количественную оценку осуществляли методом нормализации по площади пиков (полный ионный ток) идентифицированных соединений с использованием автоматической системы обработки.
Результаты исследования и их обсуждение
Всех соединений в пробах, включая неидентифицированные, насчитывается более 90 (рисунок). С помощью анализа методом ГЖХ-МС в извлечениях из ЛРС маклейи обнаружено шесть азотсодержащих соединений (таблица). Также в извлечениях были найдены соединения других классов – углеводороды С21–С25, дитерпеновый спирт фитол, который присутствует во всех зеленых растениях, эфиры фталевой кислоты, часто встречающиеся в извлечениях из ЛРС, что может быть обусловлено загрязнением почвы и воды пластиком.
Для оптимизации хроматографического разделения алкалоидных соединений проведен подбор температурной программы, выявлено, что протопиновые алкалоиды образуют паровую фазу при температуре 240 °С, как соединения близкой химической структуры они выходят близко расположенными пиками. Выявлено, что в извлечении из образцов обоих видов маклейи превалируют протопин и аллокриптопин, причем в таковом из M. сordata содержание этих соединений заметно выше, чем в M. microcarpa, что явствует из площадей пиков. Отношение содержаний протопина и аллокриптопина, вычисленное по площадям пиков, составляет в ЛРС маклейи сердцевидной – 1,6, в мелкоплодной – 1,3. Предложенная методика и полученные результаты позволяют использовать их при количественной оценке в пересчете на стандартный образец при его наличии.
В обеих пробах найдено азогетероциклическое соединение 2,4-диамино-7,8,9,10-тетрагидро-11-(3-пиридил)пиримидо[5’,4’:2’,3’]тиено[5,4-b]хинолин, оно может не являться нативным, так как при высоких температурах могут происходить различные процессы, приводящие к появлению дериватов и артефактов, которых нет в ЛРС, а именно окисление и другие процессы, приводящие к деградации соединений, перегруппировкам и т.д. В извлечении из M. сordata также найдены алкалоид дигидронитидин, а также бензо[f]бензимидазоло[2,1-b]бензотиазол и 4-амино-2-[p-(диметиламино)фенил]-5H-1]бензопирано[4,3-d]пиримидин-5-он, которые также могут как быть нативными соединениями, так и являться артефактами.
Протопиновые алкалоиды и азотсодержащие соединения Macleaya, идентифицированные методом ГЖХ-МС
|
№ |
Время удерживания |
Название вещества |
Формула вещества |
Macleaya cordata (Willd.) R. Br.) |
Macleaya microcarpa (Maxim.) Fedde |
CAS |
R. Match |
||
|
Площадь пика |
Содержание |
Площадь пика |
Содержание |
||||||
|
1 |
13.639 |
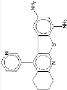
Бензо[f]бензимидазоло [2,1-b]бензотиазол |
|
54590 |
2.1 |
– |
– |
296885-53-5 |
735 |
|
2 |
13.674 |
4-Амино-2- [p-(диметиламино)фенил]-5H-[1]бензопирано[4,3-d]пиримидин-5-он |
|
198505 |
7.638 |
– |
– |
32644-52-3 |
758 |
|
3 |
15.827 |
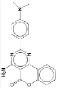
2,4-Диамино-7,8,9,10-тетрагидро-11- (3-пиридил)пиримидо [5’,4’:2’,3’]тиено [5,4-b]хинолин |
|
270672 |
10.414 |
2090 |
0.61 |
159717-99-4 |
790 |
|
4 |
31.587 |
Протопин |
|
663014 |
25.516 |
313125 |
10.798 |
485-91-6 |
800 |
|
5 |
31.623 |
Аллокриптопин |
|
393186 |
15.130 |
235150 |
8.248 |
130-86-9 |
805 |
|
6 |
34.021 |
Дигидронитидин |
|
4093 |
0.157 |
– |
– |
13063-06-4 |
772 |
Источник: составлено автором на основе полученных данных в ходе исследования.
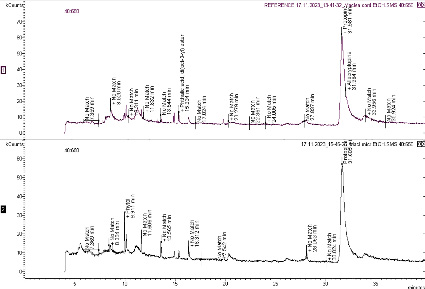
Хроматограммы извлечений из Macleaya cordata (верхняя) и Macleaya microcarpa (нижняя) Источник: составлено автором по результатам данного исследования
Существование в растении второго соединения из вышеуказанных вполне возможно, так как известно, что кольцевая система бензотиазола первоначально была обнаружена в различных морских и других природных соединениях, такие соединения широко используются в качестве антиоксидантов, регуляторов роста растений, противовоспалительных средств, ингибиторов ферментов и др. благодаря своей высокой фармацевтической и биологической активности [17].
Заключение
Предложена методика качественного обнаружения протопиновых алкалоидов в образцах травы маклейи методом ГЖХ-МС. При наличии стандартного образца анализируемые вещества можно оценивать количественно.
В извлечениях из ЛРС M. cordata и M. microcarpa обнаружено шесть азотсодержащих соединений – протопиновые алкалоиды – протопин и аллокриптопин, дигидронитидин обнаружен только в извлечении из ЛРС M. cordata.
В обеих пробах найдено азогетероциклическое соединение 2,4-диамино-7,8,9, 10-тетрагидро-11-(3-пиридил)пиримидо[5’,4’:2’,3’]тиено[5,4-b]хинолин, а также бензо[f]бензимидазоло[2,1-b]бензотиазол и 4-амино-2-[p-(диметиламино)фенил]-5H-1] бензопирано[4,3-d]пиримидин-5-он, которые также могут как быть нативными соединениями, так и являться артефактами.
Конфликт интересов
Библиографическая ссылка
Копытько Я.Ф. КАЧЕСТВЕННОЕ ОБНАРУЖЕНИЕ ПРОТОПИНА В ТРАВЕ MACLEAYA CORDATA И MACLEAYA MICROCARPA МЕТОДОМ ГАЗО-ЖИДКОСТНОЙ ХРОМАТО-МАСС-СПЕКТРОМЕТРИИ // Международный журнал прикладных и фундаментальных исследований. 2025. № 8. С. 71-76;URL: https://applied-research.ru/ru/article/view?id=13749 (дата обращения: 23.05.2026).
DOI: https://doi.org/10.17513/mjpfi.13749