Хронический лимфоцитарный лейкоз (ХЛЛ) - злокачественное клональное, лимфопролиферативное заболевание, характеризующееся накоплением атипичных зрелых CD5, CD19, CD23 - положительных В-лимфоцитов преимущественно в крови, костном мозге, лимфатических узлах, печени, селезенке [4]. ХЛЛ одно из наиболее распространенных онкогематологических заболеваний [4] и составляет около 3 случаев на 100 тыс. человек в год. Дебют заболевания как правило происходит в пожилом возрасте. Причина развития до конца не установлена. Предрасположенность к заболеванию передается по наследству (риск развития ХЛЛ у непосредственных родственников в 7 раз превышает популяционный). Большей части случаев ХЛЛ, если не всем, предшествует предлейкозное состояние (моноклональный В-клеточный лимфоцитоз), которое наблюдается у 5 – 10% людей в возрасте старше 40 лет [5]. В отличие от других B-клеточных лейкозов, для ХЛЛ не удалось выявить типичных хромосомных транслокаций, затрагивающих онкогены. Кроме того, крупные хромосомные перестройки редко наблюдаются на ранних стадиях заболевания, так что маловероятно, что они являются первичной причиной ХЛЛ. Однако по мере прогрессирования заболевания такие перестройки происходят: чаще всего это делеции участков хромосом 11, 13,17 [3]. Злокачественные клетки имеют CD19/CD5/CD23-положительный иммунофенотип и низкий уровень мембранных иммуноглобулинов. Нормальные популяции В-клеток с таким набором поверхностных маркеров неизвестны, что мешает установить, какой тип клеток может давать начало злокачественному клону при ХЛЛ. Анализ транскриптома показал, что опухолевые клетки по набору синтезируемых мРНК похожи на зрелые В-клетки, которые прошли активацию антигеном. В норме таким профилем экспрессии генов обладают В-клетки памяти и В-клетки краевой зоны лимфатических фолликулов, поэтому предполагают, что именно они могут быть предшественниками лейкозных клеток [5]. Развитие ХЛЛ под влиянием канцерогенных химических веществ и ионизирующего излучения как этиологических факторов не доказано. Тем не менее, в клинической практике врачи сталкиваются с подобными неординарными случаями.
Целью настоящего исследования явилось выявление влияния соединений ртути в качестве этиологического фактора развития ХЛЛ.
Клинический случай.
В хирургическое отделение краевой клинической стоматологической поликлиники обратилась пациентка Щ., 42 лет, с жалобами на слабость, недомогание, болезненность и дискомфорт во 2 квадранте зубочелюстной системы. Из анамнеза установлено, что около 2х лет назад проводилась радикальная гайморотомия слева, по поводу радикулярной кисты с прорастанием от 24 зуба с одновременной резекцией верхушек корней и их ретроградным пломбированием амальгамой. Через неделю после операции возникло воспалительное осложнение в виде серозно-гнойного гайморита. Было проведено противовоспалительное лечение и экстракция 24 зуба. Процесс купировался.
До вмешательства больная считала себя здоровым человеком с нормальными регулярно контролируемыми клинико-лабораторными показателями. Сохраняющиеся продромальные явления астенического типа вызвали необходимость послеоперационного обследования. При интерпретации общего анализа крови было обнаружено существенное увеличение лейкоцитов (68 тыс./мл), относительного содержания лимфоцитов (52%). После консультации гематолога был выставлен диагноз – ХЛЛ. Больная получала заместительную симптоматическую терапию. Диагноз был подтвержденв гематологическом научном центре РАМН и в Израиле. При иммунофенотип ии была выявлена экспрессия маркеров В-лимфоцитов (CD5, CD19, CD23). Планировались варианты лечения как химиотерапия, иммунотерапия , трансплантация костного мозга . В ходе обследования была проведена конусно-лучевая компьютерная томография (КЛКТ), выявлены множественные инородные включения в области операционного вмешательства. Было принято решение санировать данную область.
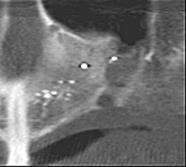
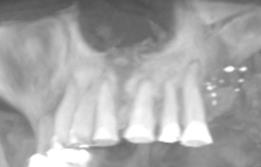
При обследовании стоматологического статуса существенных изменений обнаружено не было. Кожные покровы, открывание рта, глотание – без особенностей. В подчелюстной области пальпировался одиночный слабо-болезненный подвижный лимфоузел эластической консистенции, размером примерно 0,8х0,6 мм. Носоротовая проба отрицательна. 24 зуб отсутствует. Слизистая оболочка полости рта в области 23-26 зубов достаточно увлажнена, незначительно болезненна при пальпации, бледно-розового цвета, из-под нее просвечиваются темно-синие пятна. При анализе ортопантомограммы (ОПГ) и конусно-лучевой компьютерной томограммы (КЛКТ) подтверждено наличие множественных милиарных металлинизированных включений, располагающихся с вестибулярной поверхности альвеолярного отростка (рис.1,2).
|
Рис. 1. Ортопантомограмма пациентки Щ, 42 г. при обследовании |
Рис. 2. Компьютерная томограмма пациентки Щ., 42 г. при обследовании |
Был выставлен диагноз – Множественные инородные тела верхней челюсти в области 24-25 зубов.
После подготовки, включающей прием коагулянтов непрямого действия и предоперационно – дицинон, в/м 2мл, препарирован слизисто-надкостничный лоскут в области 23-26 зубов. На наружной поверхности кости обнаружены инородные блестящие включения темного цвета, которые были удалены механически. Визуально препарированное костное ложе осталось "чистым". Внутренняя поверхность мобилизованного лоскута оказалась сплошь пропитанной диффузно расплывчатыми металлинизированными включениями, не имеющими каких-либо границ между собой. В связи с этим было принято решение о тотальном иссечении надкостницы с сохранением мукогингивального лоскута путем его послойного продольного рассечения. Оставшаяся слизистая сохранила свою целостность и не отличалась по цвету с окружающими тканями. Постоперационные костные дефекты альвеолярного отростка компенсированы "Bio-Oss" и закрыты резорбируемой мембраной "Bio-Gide" (Geistlich). Рана герметично ушита ПГА. На контрольных ОПГ и КЛКТ следов амальгамы не обнаружено (рис.3,4).
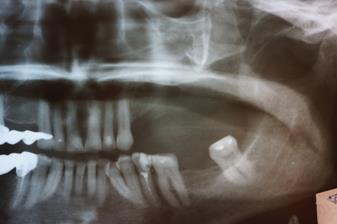
Рис. 3. Ортопантомограмма пациентки Щ., 42 г. после оперативного вмешательства
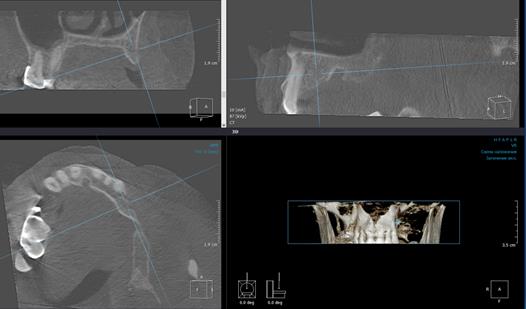
Рис. 4. Компьютерная томограмма пациентки Щ., 42 г. после оперативного вмешательства
Послеоперационный период протекал удовлетворительно.
Через 2 месяца больная жалоб местного характера не предъявляла. При осмотре патологии со стороны ЧЛО не выявлено. При сборе анамнеза установлено, что за прошедший период улучшилось общее состояние, лейкоцитоз снизился вдвое, уменьшилось процентное содержание лимфоцитов. В связи с этим в гематологическом центре принято решение об активном динамическом наблюдении. Обследование через 1 и 2 года констатироваили стабильно удовлетворительное состояние.
Заключение
Таким образом, установлено, что ХЛЛ может быть детерминирован контактом с ртутью. Предположительным механизмом возникновения ХЛЛ может быть развитие хронического микро- и меркуриализма [1,2]. В основе патогенеза отравления и действия ртути лежит блокада биологически активных групп белковой молекулы (сульфгидрильных, аминных, карбоксильных и др.), изменения мембраны эндоплазматического ретикулума, включение ртути в молекулу т-РНК. По-видимому, последнее и является непосредственной основой делеции участков хромосом. Учитывая возможные осложнения, ассоциированные с амальгамами и наличие альтернативных стоматологических препаратов, необходимо в схеме хирургического протокола пользоваться последними как императивом.
Библиографическая ссылка
Цымбалов О.В. НОВЫЕ ПРЕДСТАВЛЕНИЯ НА ЭТИОЛОГИЮ ЛИМФОЛЕЙКОЗА И ЗНАЧЕНИЕ СТОМАТОЛОГИЧЕСКОЙ САНАЦИИ // Международный журнал прикладных и фундаментальных исследований. 2014. № 2. С. 205-209;URL: https://applied-research.ru/ru/article/view?id=4727 (дата обращения: 28.04.2026).