Проблема совершенствования медицинской помощи больным с повреждениями опорно-двигательной системы с каждым годом приобретает всё большее значение, в связи с ростом числа пострадавших и увеличением уровня инвалидности от травм у лиц трудоспособного возраста и детей [4]. За последнее столетие широкое распространение получили методы оперативного лечения переломов. Предложены внутренние (внутрикостные и накостные) и внешние (спицевые и стержневые) фиксаторы для обеспечения максимально надежного остеосинтеза сломанной кости. Однако не всегда современные методы лечение являются успешными, а сроки консолидации остаются длительными [6].
В последние годы наметилась активная тенденция в разработке биоматериалов, направленных на стимуляцию репаративных процессов в поврежденных тканях [1, 10].
Имея опыт применения flexible intramedullary nailing при удлинении конечностей [5, 9], позволивший нам сократить длительность внешней фиксации и количество костных и септических осложнений, мы применяем с 2001 года аппарат и метод Илизарова в сочетании с интрамедуллярными эластичными спицами у лиц с повреждениями длинных костей [3].
Целью данного исследования явилось экспериментальное сравнение рентгеноморфологических особенностей репаративного остеогенеза при диафизарных переломах длинных костей в условиях чрескостного остеосинтеза по Илизарову и комбинированного чрескостного остеосинтеза с интрамедуллярным армированием спицами.
Материалы и методы исследования
Были выполнены две группы экспериментальных исследований на 20 взрослых беспородных собаках обоего пола. Возраст животных варьировал в диапазоне 1-5 лет.
Во всех случаях в условиях операционной наркотизированным животным моделировали открытый поперечный перелом костей голени. Костные отломки фиксировали аппаратом Илизарова. В 1 группе экспериментов дополнительной фиксации не производили. Во 2 группе дополнительно выполняли армирование большеберцовой кости двумя спицами.
С этой целью были использованы спицы толщиной 1,8 мм из титанового сплава с покрытием из гидроксиапатита толщиной 20-40 мкм и пористостью 2-8 %, полученное методом анодного оксидирования в дуговом режиме. Покрытие представляло собой многоуровневую ультрапористую систему, состоящую из макро- и микропор от 50-100 нм до 1-2 мкм в диаметре. Спицы вводили с медиальной и латеральной стороны в области шероховатости гребня большеберцовой кости до уровня дистального метафиза и затем скусывали под основание, мягкие ткани в области раны зашивали наглухо. Спицы, введенные в костномозговой канал, не извлекали на протяжении всего эксперимента.
Для оценки особенностей течения репаративного остеогенеза в созданных условиях использовали рентгенографический, гистологический и статистический методы исследования.
Рентгенографию костей голени выполняли в двух стандартных проекциях (прямой и боковой) перед оперативным вмешательством, непосредственной после остеосинтеза, далее через 7, 14, 28, 45 и 75 суток эксперимента. Использовали рентгеновский аппарат «VEP X Technology Premium VET» (Испания).
Гистологические исследования выполняли в периоды 14, 28, 45 и 75 суток опыта. Для этого участки диафизов оперированных костей распиливали в продольном и поперечном направлениях, фиксировали в 10 % растворе нейтрального формалина и заливали в целлоидин. Гистотопографические срезы окрашивали гематоксилином-эозином и пикрофуксином по Ван-Гизону. Исследование репаративной регенерации костной ткани осуществляли методом световой микроскопии с использованием микроскопа «Никмед-5» («ЛОМО», Санкт-Петербург, Россия). Для получения микрофото гистологических препаратов использовали аппаратно-программный комплекс «ДиаМорф» (Москва, Россия), смонтированный на базе большого исследовательского фотомикроскопа («OPTON», Германия).
Для оценки полученных количественных данных использовали метод описательной статистики (вычисляли среднее значение и стандартное отклонение). Обработку результатов выполняли с использованием программы «AtteStat 13.1» (И.П. Гайдышев, Россия).
Эксперименты выполнены в соответствии с требованиями «Европейской конвенции по защите позвоночных животных, используемых для экспериментальных и других научных целей» и были одобрены Комитетом по этике ФГБУ «РНЦ «ВТО» им. акад. Г.А. Илизарова».
Результаты исследования и их обсуждение
Рентгенография. В 1 серии экспериментов через 7 суток фиксации (рис. 1а) на рентгенограммах признаки репаративной регенерации в области остеотомии не определялись. Контуры концов костных отломков были ровными, четкими. Признаки периостальной и эндостальной реакции отсутствовали.
Через 14 суток (рис. 1b) появлялись первые признаки репаративонй реакции. Контуры концов отломков были менее четкими по сравнению с предыдущим сроком обследования. На проксимальном и дистальном костных отломках в области остеотомии наблюдали тени периостальной реакции толщиной 1,7±0,4 мм и протяженностью 4,3±0,6 мм, которые не объединялись между собой. В проекции костномозговых каналов отломков появлялись тени эндостального происхождения протяженностью до 2,5 мм по высоте от уровня остеотомии.
Через 30 суток фиксации (рис. 1с) контуры концов отломков были нечеткие. Межфрагментарная щель определялась ввиде ровной полосы просветления, которую перекрывали тени гомогенной структуры. В проекции костномозговых полостей были тени эндостального регенерата протяженностью до 3,4-3,6мм. Периостальные образования, высотой не более 1,2 мм находились в стадии компактизации и в 80 % наблюдений в виде муфты объединяли отломки в зоне их стыка с трех сторон.
Через 45 суток фиксации (рис. 1d) на рентгенограммах наблюдали признаки полного костного сращения. Линия остеотомии слабо определялась и была перекрыта тенями, интенсивность которых приближалась к интенсивности близлежащих участков. Тени эндостального регенерата в проекции формирующейся единой костномозговой полости определялись только около концов отломков. Периостальные разрастания заметно компактизировались или подвергались полной редукции. В этот период аппарат Илизарова демонтировали.
Через 75 суток опыта (30 суток после прекращения фиксации аппаратом) ось кости была правильная (рис. 1i). Линия остеотомии слабо определялась. Была сформирована единая костномозговая полость и непрерывная корковая пластинка. Эндостальная и периостальная реакции в области остеотомии не выявлялись.
Во 2 группе опытов на рентгенограммах через 7 суток фиксации (рис. 2a) появлялись первые признаки репаративного остеогенеза, что характеризовалось появлением вуалевидных теней периостального происхождения в области стыка костных отломков. Линия остеотомии определялась в виде полосы просветления с нечеткими контурами.
Через 14 суток после остеосинтеза (рис. 2b) контуры концов отломков были размыты. Линия перелома слабо определялась. В проекции костномозговых полостей отломков были хорошо выражены тени эндостальной реакции на протяжении всей длины интрамедуллярного имплантата. Периостальные наслоения в проекции зоны перелома были представлены тенями с неровными, нечеткими контурами толщиной 2,8±0,2 мм и протяженностью 14,7±1,3 мм. В 60 % наблюдений периостальные наслоения перекрывали линию перелома с краниальной и каудальной поверхности, что свидетельствует о практической консолидации отломков.

Рис. 1. Фрагменты рентгенограмм, 1 группа, после остеотомии: а – через 7 суток, b – через 14 суток, с – через 30 суток, d – через 45 суток, i – через 75 суток эксперимента
Через 30 суток фиксации (рис. 2c) на рентгенограммах выявляли полное костное сращение перелома. Контуры концов отломков сливались с линией остеотомии, в результате чего последняя практически не определялась. Компактизированные периостальные наслоения объединяли проксимальный и дистальный отломки между собой со всех сторон. Эндостальная реакция наблюдалась вдоль всей длины внутрикостных спиц. В этот период прекращали фиксацию аппаратом Илизарова.
Через 45 суток фиксации (рис. 2d) на рентгенограммах линия остеотомии была представлена единичными участками просветления. Тени эндостальной реакции определялись вдоль внутрикостно-расположенных спиц. Периостальные наслоения подвергались редукции.
Через 75 суток опыта (рис. 2i) на рентгенограммах завершалось формирование непрерывной корковой пластинки и единой костномозговой полости. Однако тени в проекции костномозгового канала были более рентгеноконтрастные. Линия остеотомии и периостальная реакция на отломках не определялись.
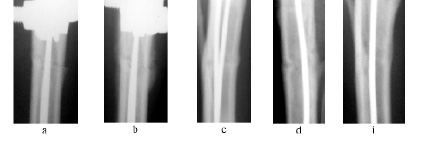
Рис. 2. Фрагменты рентгенограмм, 2 группа, после остеотомии: а – через 7 суток, b – через 14 суток, с – через 30 суток, d – через 45 суток, i – через 75 суток эксперимента
Гистологическое исследование. В 1 группе экспериментов (рис. 3) через 14 суток фиксации в интермедиарной области определяли тяжи рыхлой волокнистой соединительной ткани. Периостальный регенерат состоял из среднеячеистой губчатой кости с участками неминерализованной соединительной ткани. Проксимальный и дистальный периостальные регенераты не объединялись. Эндостальная область регенерата была представлена среднепетлистой и крупнопетлистой губчатой костью с участками хондроида и волокнистого хряща.
Через 30 суток на гистологических препаратах определяли эндостальная консолидация отломков большеберцовой кости. В щели между отломками определяли массивные ретикулофиброзные трабекулы губчатой кости и рыхлую волокнистую соединительную ткань межтрабекулярных пространств. Периостально образованная губчатая кость подвергалась компактизации. На отдельных участках проксимальный и дистальный периостальные регенераты объединялись между собой.
Через 45 суток фиксации гистологически определяли полное костное сращение перелома. В периостальной, интермедиарной и эндостальной областях зоны сращения располагалась ретикулофиброзная губчатая кость с красным костным мозгом в межтрабекулярных пространствах.
Через 75 суток (30 суток после прекращения фиксации аппаратом) между отломками наблюдали костное сращение. В интермедиарной области между отломками была сформирована пластинчатая костная ткань. Новообразованная корковая пластинка имела остеонное строение. Однако ориентация остеонов еще не соответствовала норме. В единой костномозговой полости содержался гемопоэтически-жировой мозг.

Рис. 3. Микрофото межотломкового пространства в интермедиарной области 1 группа, после остеотомии: а – через 14 суток, b – через 30 суток, с – через 45 суток, d – через 30 суток после прекращения фиксации аппаратом (75 суток эксперимента). Препараты (a, с, d) окрашены гематоксилином и эозином, b – пикрофуксином по Ван-Гизону. Увеличение – 25х (a, b, d), с – 63х
Во 2 группе экспериментов (рис. 4) через 14 суток после операции гистологическая картина соответствовала первой серии экспериментов. Кроме этого вокруг интрамедуллярных спиц на протяжении всей их длины формировался костный футляр, который сохранялся до конца эксперимента. Он состоял из тонкой остеоидной капсулы толщиной 30-40 мкм, циркулярно ориентированных пластин компактной кости. В межтрабекулярном пространстве костного футляра располагались участки грануляционной ткани с многочисленными сосудами и периваскулоцитами на различных этапах остеогенной дифференцировки.
Через 30 суток эксперимента видно полное периостальное, интермедиарное и эндостальное костное сращение. В интермедиарном пространстве определялись участки губчатой и зрелой пластинчатой костной ткани. Периостальные наслоения образованные мелкопятлистой сетью костных трабекул пластинчатого строения объединяли костные отломки между собой. Полностью сформировано компактное вещество большеберцовой кости. В костном футляре вокруг спиц наблюдали преобразование грубоволокнистой костной ткани в более минерализованную зрелую пластинчатую, а футляр консолидировался с эндостальной поверхностью (рис. 5).
Через 45 суток после остеосинтеза в интермедиарном пространстве концы отломков были соединены узкопетлистой сетью костных трабекул и остеонами различной степени зрелости с явлениями компактизации по всей ширине кортикального слоя. Костный футляр вокруг спиц был образован компактной костью пластинчатого строения с формирующимися остеонами и губчатой костной тканью, которая распространялась не только в диастаз, но и заполняла костномозговую полость отломков, скрепляя их подобно штифту.
Через 75 суток эксперимента на гистотопограммах регенерат имел более органотипичное строение по сравнению с 1 группой опытов.
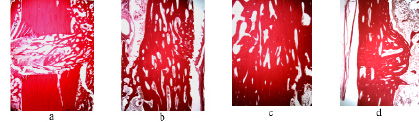
Рис. 4. Микрофото межотломкового пространства в интермедиарной области 2 группа, после остеотомии: а – через 14 суток, b – через 30 суток, с – через 45 суток, d – через 30 суток после прекращения фиксации аппаратом (75 суток эксперимента). Препараты (a-d) окрашены гематоксилином и эозином. Увеличение – 12,5х
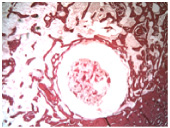
Рис. 5. Микрофото поперечного среза костномозгового канала вне зоны перелома: 30 дней после перелома – вокруг спицы сформирован костный футляр, срастание с костной тканью на эндостальной поверхности отломка большеберцовой кости. Окраска гематоксилином и эозином, увеличение – х2,5
Известно, что при диафизарных переломах длинных трубчатых костей, основным методом остеосинтеза в большинстве стран является интрамедуллярный. Внутрикостные штифты и гвозди делают из нержавеющей стали или титана по форме и размерам приближающиеся к форме костномозгового канала (треугольный или круглый). Основная цель – обеспечить полную неподвижность костных фрагментов, что должно позволить перейти к более ранней нагрузке на оперированную конечность.
Основным недостатком интрамедуллярного остеосинтеза считается повреждение сосудов и системы кровообращения медуллярного канала, разрушение костного мозга и эндоста, что значительно ослабляет остеогенные потенции плюрипотентных клеток стромы костного мозга. Отмечена и опасность инфекционного осложнения при лечении открытых переломов, при интрамедуллярном остеосинтезе [8].
Альтернативой для разрушающего влияния интрамедуллярных стержней стал остеосинтез аппаратом Илизарова, однако громоздкие некомфортные для пациента внешние опоры и необходимость длительной фиксации (в течение нескольких месяцев) не способствуют популярности данного метода среди врачей и пациентов.
Идеальным разрешением данного противоречия мог бы стать полностью биосовместимый внутрикостный имплантат, который выполняет все пространство костномозгового канала и срастается с эндостом, обеспечивает внутрикостное кровообращение не повреждая a. nutricia и обладает всеми морфологическими качествами натуральной аутокости.
Решение данной задачи мы находим в использовании комбинированного остеосинтеза. Гистологические экспериментальные исследования показали, что через 14 суток после операции вокруг интрамедуллярных спиц на протяжении всей их длины формируется костный футляр, который сохраняется до конца эксперимента. Он состоит из тонкой остеоидной капсулы толщиной 30-40 мкм, циркулярно ориентированных пластин компактного вещества кости, образующихся за счет аппозиционного костеобразования на поверхности спиц и примыкающих к ним трабекул губчатой кости. Через 14-21 сутки после операции большая часть пространства костномозгового канала вокруг спиц заполнено губчатым костным веществом, муфтообразное скопление пучков коллагеновых волокон плоской, лентовидной формы, располагаются в продольном и циркулярном направлениях. Пучки коллагеновых волокон остеоида прочно фиксированы к шероховатой, наноструктурированной поверхности покрытия спиц и связаны с эндостальной поверхностью кости – формируется своебразный костный штифт, обеспечивающий раннюю консолидацию фрагментов и надежную их фиксацию. В межтрабекулярном пространстве костного футляра располагаются участки грануляционной ткани с многочисленными сосудами. Основной ствол внутрикостной артерии никогда не повреждается.
В этот период отмечается активный костеобразовательный процесс с вектором роста трабекул, направленным в сторону диастаза, выражающийся в массовой пролиферации остеогенных клеток периоста, эндоста и костного футляра вокруг спиц и образовании значительных по объему периостальных и эндостальных (в большей степени) костно-остеоидных разрастаний, перекрывающих диастаз.
Регенерат располагается по всему поперечнику кости. В интермедиарной зоне локализуются кровеносные сосуды и многочисленные анастомозирующие трабекулы ретикулофиброзной костной ткани, врастающие навстречу друг другу с периостальной и эндостальной (в большей степени) поверхностей и образующие напластования на концы отломков. Образуется первичное эндостально-периостальное и интермедиарное сращение.
Через 28 суток после операции концы отломков теряют четкие границы из-за массивных отложений в интермедиарном пространстве зрелой пластинчатой костной ткани, плотно спаянной с кортикальным слоем костных фрагментов. Наблюдается фаза органогенеза и ремоделирования, о чем свидетельствует перестройка первичных трабекул в органотипические остеонные структуры, формирующие кортикальный слой.
Через 45 суток после операции концы отломков соединены в интермедиарном пространстве узкопетлистой сетью костных трабекул и остеонами различной степени зрелости с явлениями компактизации по всей ширине кортикального слоя. Заживление перелома происходит по типу первичного за счет врастания в диастаз от концов отломков по ходу кровеносных сосудов остеогенных клеток гаверсовых каналов, формирующих костные трабекулы и остеоны, располагающиеся поперек линии излома. Костный футляр вокруг спиц образован компактной костью пластинчатого строения с формирующимися остеонами и губчатой костной тканью, которая распространяется не только в диастаз, но и заполняет костномозговую полость отломков, скрепляя их подобно штифту.
Процесс репаративного остеогенеза при фиксации перелома только аппаратом Илизарова отстает на 2-3 недели. Интенсивность костеобразования в этом случае ограничена в основном зоной перелома. Эндостальная и периостальная реакция видна только на протяжении 2,5-4 мм от линии перелома, в интермедиарной зоне отмечается хондроид и волокнистый хрящ. Во второй группе эксперимента консолидация перелома осуществляется в ранние сроки по первичному типу без образования хрящевой и соединительной ткани в костной спайке.
С нашей точки зрения интрамедуллярные спицы обеспечивают не только дополнительную стабильность костных отломков. Покрытие поверхности титановых имплантатов наноструктурированным высокопористым слоем гидроксиапатита обеспечивает высокую биосовместимость с тканевыми структурами регенерата, увеличивает скорость остеоинтеграции и предотвращает образование фибриллярной соединительной ткани и хряща в регенерате [2, 7]. Вокруг спиц образуется зона активного аппозиционного костеобразования и формируется костный футляр со свойствами кондуктора и индуктора остеогенеза, обеспечивающий направленный рост костной ткани, пролонгированную стимуляцию ангиогенеза и репаративного костеобразования.
Заключение
Таким образом, результаты исследования свидетельствуют о положительном влиянии интрамедуллярных спиц с покрытием из гидроксиапатита на течение и интенсивность репаративного костеобразования при заживлении перелома. Полученные данные позволяют рекомендовать данный сравнительно малоинвазивный способ оптимизации остеорепарации для применения в комплексе с другими методами консервативного и оперативного лечения перелома кости, особенно при вялотекущих репаративных процессах у детей, пациентов пожилого и старческого возраста, а также у ослабленных больных.
Работа выполнена при частичной финансовой поддержке Федеральной целевой программы «Исследования и разработки по приоритетным направлениям развития научно-технологического комплекса России на 2014-2020 годы» (ГК 14.577.21.0036), гранта РФФИ 13-08-98052 р_сибирь_а.
Библиографическая ссылка
Попков А.В., Попков Д.А., Ирьянов Ю.М., Кононович Н.А., Горбач Е.Н., Твердохлебов С.И. CТИМУЛЯЦИЯ РЕПАРАТИВНОЙ РЕГЕНЕРАЦИИ КОСТНОЙ ТКАНИ ПРИ ДИАФИЗАРНЫХ ПЕРЕЛОМАХ (ЭКСПЕРИМЕНТАЛЬНОЕ ИССЛЕДОВАНИЕ) // Международный журнал прикладных и фундаментальных исследований. 2014. № 9-1. С. 82-88;URL: https://applied-research.ru/ru/article/view?id=5794 (дата обращения: 30.04.2026).

