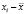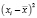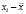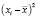Валидация в соответствии с Правилами GMP – это действия, которые доказывают, что определенная методика, процесс, оборудование, сырье, деятельность или система действительно приводят к ожидаемым результатам [5].
Согласно российского стандарта ГОСТ Р ИСО 9000-2008, понятие валидация определена как подтверждение посредством представления объективных свидетельств того, что требования, предназначенные для конкретного использования или применения, выполнены [4].
Основой для проведения процедуры валидации служат методы статистической обработки результатов анализа, достаточно популярно изложенные применительно к области фармации в ряде публикаций [1, 6], на которые и опираются авторы данной статьи.
Валидация метода контроля качества – это процесс установления характеристик метода, показателей его эффективности и определения его ограничений [6]. Главной задачей валидации аналитической методики является экспериментальное доказательство того, что данная методика пригодна для достижения тех целей, для которых она предназначена. При валидации аналитических методов в фармации в основном используют такие метрологические характеристики, как прецизионность, точность, воспроизводимость, повторяемость, правильность, чувствительность, устойчивость, линейность.
Основной характеристикой аналитических методик для количественного определения лекарственных средств и количественной оценки примесей является прецизионность.
Прецизионность является общим термином для выражения изменчивости повторяющихся измерений. Согласно ГОСТ прецизионность – это степень близости друг к другу независимых результатов измерений, полученных в конкретных регламентированных условиях [3].
Прецизионность аналитической процедуры выражает близость значений (степень разброса) между сериями измерений, полученных в результате многократного анализа одного и того же образца при заданных условиях.
Она выражается как коэффициент вариации в % (относительное стандартное отклонение, %RSD) для статистически значимого количества образцов (n ≥ 10).
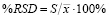 , (1)
, (1)
где S – среднеквадратическое отклонение экспериментальных величин,
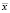 – концентрация анализируемого вещества (среднее значение).
– концентрация анализируемого вещества (среднее значение).
Среднеквадратичное отклонение от среднего (стандартное отклонение выборки, S) является мерой рассеяния (дисперсии) результатов измерений и рассчитывается по формуле (2):
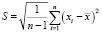 , (2)
, (2)
где xi – результат эксперимента.
В измерениях принято использовать несколько типов прецизионности, в частности таких, как: повторяемость (сходимости, r) и воспроизводимость (R) результатов.
Повторяемость выражает прецизионность при одинаковых рабочих условиях на протяжении короткого промежутка времени, то есть является мерой прецизионности при выполнении ряда условий:
– работает один и тот же исследователь,
– используется один и тот же прибор,
– используется один и тот же метод,
– анализы выполняются в течении короткого промежутка времени,
– используется идентичный объект испытания,
– исследования проводятся в одной и той же лаборатории.
Мерой повторяемости является стандартное отклонение повторяемости (Sr ) и предел повторяемости (r). Предел повторяемости (сходимости) – это значение, которое с доверительной вероятностью 95 % не превышается абсолютной величиной разности между результатами двух измерений (или испытаний), полученными в условиях повторяемости (сходимости).
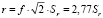 , (3)
, (3)
где f – коэффициент критического диапазона.
Величина f (коэффициент критического диапазона) зависит от доверительного уровня вероятности и закона распределения случайной величины. Для пределов воспроизводимости и повторяемости доверительный уровень вероятности составляет 95 %, и в ГОСТ Р ИСО 5725 делается допущение, что лежащее в основе распределение является приближенно нормальным. Для нормального распределения на уровне вероятности 95 % коэффициент равен 1,96 [3].
Воспроизводимость результатов выражает прецизионность, оцененную по результатам, полученным разными исследователями (внутрилабораторная) или в разных лабораториях (межлабораторная) при выполнении ряда условий:
– работают разные исследователи,
– используется один и тот же метод,
– используется идентичный объект испытания,
– исследования проводятся в одной и той же (внутрилабораторная) или разных лабораториях.
При внутрилабораторных испытаниях прецизионности наблюдения осуществляются в одной и той же лаборатории, но при этом один или несколько факторов – «время», «оператор» или «оборудование» – могут меняться. При установлении прецизионности метода измерений очень важно точно определить соответствующие условия наблюдения, т.е. должны ли быть три вышеупомянутых фактора неизменными или нет. Внутрилабораторные испытания в различные моменты времени учитывают влияние изменения условий окружающей среды и перекалибровки оборудования между наблюдениями. Если в условиях повторяемости наблюдения осуществляются при неизменности всех внутрилабораторных факторов, то в условиях воспроизводимости эти факторы наоборот изменчивы. Если наблюдения выполняются в различных лабораториях, проявляются дополнительные эффекты, являющиеся следствием различия между лабораториями (в административном управлении, материально-техническом обеспечении, проверке стабильности наблюдений и т.д.).
Мерой воспроизводимости является стандартное отклонение воспроизводимости (SR ) и предел воспроизводимости (R = 2,77 SR).
Необходимость рассмотрения прецизионности по ГОСТ Р ИСО 5725-2002 [3] возникает из-за того, что измерения, выполняемые на предположительно идентичных материалах, при предположительно идентичных обстоятельствах, не дают, как правило, идентичных результатов. Это объясняется неизбежными случайными погрешностями, присущими каждой измерительной процедуре, а факторы, оказывающие влияние на результат измерения, не поддаются полному контролю. При практической интерпретации результатов измерений эта изменчивость должна учитываться. Различия между результатами измерений, выполняемых разными операторами и/или с использованием различного оборудования, как правило, будут больше, чем между результатами измерений, выполняемых в течение короткого интервала времени одним оператором с использованием одного и того же оборудования.
Как применяются методы валидации в фармацевтическом анализе, можно проанализировать на примере анализа спирта этилового, который осуществляется в соответствии с ГОСТ Р 51698-2000, изм.1 «Газохроматографический экспресс-метод определения содержания токсичных микропримесей» [2].
Целью исследования является:
– доказательство пригодности метода для оценки качества лекарственных средств в соответствии с требованиями нормативных документов в условиях Испытательной контрольно-аналитической лаборатории ГУЗ «Центр сертификации и контроля качества лекарственных средств Рязанской области»;
– определение характеристики прецизионность, которая включает два показателя: повторяемость и воспроизводимость;
– разработка Стандартной операционной процедуры (СОП) «Валидация газохроматографического метода испытаний спирта этилового 95 %».
Газохроматографический метод применяется для анализа летучих веществ, либо веществ, которые могут быть переведены в парообразное состояние. В газовом хроматографе происходит разделение токсических микропримесей, содержащихся в спирте этиловом и последующее их детектирование пламенно-ионизационным детектором. В нашем случае применяется метод абсолютной градуировки, основанный на предварительном определении зависимости между количеством введенного вещества и площадью пика на хроматограмме. Полученная хроматограмма служит основой для качественного и количественного анализа токсических микропримесей в спирте этиловом.
Определение показателя «Повторяемость» выполняется одним провизором-аналитиком путем анализа 10 проб одного и того же образца трех серий спирта этилового 95 %.
Определение показателя «Воспроизводимость» оценивается по результатам анализов, выполненными параллельно двумя провизорами-аналитиками путем анализа 10 проб одного и того же образца трех серий спирта этилового 95 %.
Для примера приведены результаты испытания одной серии спирта этилового одним аналитиком по количественному содержанию метанола (табл. 1) и пропанола-2 (табл. 2) в анализируемом образце. По результатам испытаний проведён расчет среднеквадратичного отклонения (Sr) и коэффициента вариации ( %RSD). Результаты остальных испытаний по показателю повторяемости сведены в табл. 3. Результаты испытаний по показателю воспроизводимости сведены в табл. 4, по результатам испытаний проведён расчет среднеквадратичного отклонения (SR) и коэффициента вариации ( %RSD).
Таблица 1
Результаты анализа одного образца этилового спирта 95 % на содержание метанола, проведенные одним провизором-аналитиком
|
№ анализа |
Содержание метанола, об. %, xi |
|
|
|
1 |
1,8275*10-3 |
– 0,0395*10-3 |
0,00156*10-6 |
|
2 |
1,8444*10-3 |
0,0226*10-3 |
0,000511*10-6 |
|
3 |
1,7779*10-3 |
0,089*10-3 |
0,007921*10-6 |
|
4 |
1,9315*10-3 |
– 0,0645*10-3 |
0,00416*10-6 |
|
5 |
1,8158*10-3 |
0,0512*10-3 |
0,002621*10-6 |
|
6 |
1,9028*10-3 |
– 0,0358*10-3 |
0,001282*10-6 |
|
7 |
1,986*10-3 |
– 0,119*10-3 |
0,014161*10-6 |
|
8 |
1,8702*10-3 |
– 0,0032*10-3 |
0,00001*10-6 |
|
9 |
1,8275*10-3 |
0,0395*10-3 |
0,00156*10-6 |
|
10 |
1,8670*10-3 |
– 0,019*10-3 |
0,000361*10-6 |
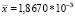
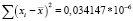
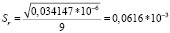
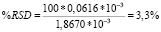
Заключение: коэффициент вариации ( %RSD) для 10 измерений по метанолу составил 3,3 %, что соответствует требованиям ГОСТ (не более 5 %) [3].
Таблица 2
Результаты анализа одного образца этилового спирта 95 % на содержание пропанола-2, проведенные одним провизором-аналитиком
|
№ анализа |
Содержание пропанола-2, мг/дм3, xi |
|
|
|
1 |
2,88*10-4 |
0,12*10-4 |
0,014*10-8 |
|
2 |
2,82*10-4 |
0,06*10-4 |
0,003*10-8 |
|
3 |
2,68*10-4 |
– 0,085*10-4 |
0,007*10-8 |
|
4 |
2,6*10-4 |
– 0,16*10-4 |
0,025*10-8 |
|
5 |
2,77*10-4 |
0,008*10-4 |
0,00006*10-8 |
|
6 |
2,8*10-4 |
0,066*10-4 |
0,004*10-8 |
|
7 |
2,79*10-4 |
0,028*10-4 |
0,00008*10-8 |
|
8 |
2,84*10-4 |
0,077*10-4 |
0,006*10-8 |
|
9 |
2,66*10-4 |
0,097*10-4 |
0,009*10-8 |
|
10 |
2,75*10-4 |
0,01*10-4 |
0,00009*10-8 |
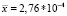
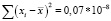
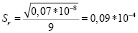

Заключение: коэффициент вариации (RSD) для 10 измерений по содержанию пропанола-2 составил 11,6 %, что соответствует требованиям ГОСТ (не более 5 %) [3].
Таблица 3
Результаты расчета по показателю «повторяемость» (сходимость) испытаний по каждой из серий спирта этилового 95 % по содержанию метанола и пропанола-2
|
условный № серии |
№ аналитика |
%RSD по содержанию метилового спирта |
%RSD по содержанию других токсических микропримесей |
|
1 |
1 |
3,3 |
4,6 |
|
2 |
1 |
4,9 |
5,0 |
|
3 |
1 |
4,8 |
2,9 |
|
1 |
2 |
4,7 |
4,2 |
|
2 |
2 |
3,5 |
4,8 |
|
3 |
2 |
2,4 |
3,2 |
Заключение: коэффициенты вариации (RSD) по метиловому спирту и по содержанию других токсических микропримесей соответствует ГОСТ (не более 15 %) [3].
Аналогично произведен расчет по содержанию пропанола-2, коэффициент вариации ( %RSD) составил 5,79 % что соответствует требованию ГОСТ – должен быть не более 7 % [3].
Из результатов испытаний, проведенных двумя аналитиками в одной и той же лаборатории на одном и том же приборе, следует, что показатели повторяемости (сходимости) и воспроизводимости не превышают указанные пределы, установленные ГОСТ.
Повторная валидация обычно проводится при изменении условий проведения метода и по истечении определенного промежутка времени, в данном случае организация установила срок проведения повторной плановой валидации через пять лет.
Таблица 4
Результаты расчета по показателю «воспроизводимость» по одной из серий спирта этилового 95 % по содержанию метанола
|
Испытатель |
Содержание спирта метилового, %
(среднее из 10 анализов), |
|
|
|
Аналитик № 1 |
1,867*10-3 |
– 0,005*10-3 |
0,000025*10-6 |
|
Аналитик № 2 |
1,877*10-3 |
0,005*10-3 |
0,000025*10-6 |




Заключение: коэффициент вариации ( %RSD) составил по метанолу 0,38 % , что соответствует требованию ГОСТ – должен быть не более 6 % [3].
Выводы
Пригодность метода для оценки качества спирта этилового 95 % в соответствии с требованиями нормативных документов (ОФС) в условиях Испытательной контрольно-аналитической лаборатории ГУЗ «Центр сертификации и контроля качества лекарственных средств Рязанской области» подтверждена характеристикой «Прецизионность», которая включает два показателя – повторяемость и воспроизводимость. Разработана Стандартная операционная процедура (СОП) «Валидация газожидкостного метода испытаний спирта этилового 95 %», обеспечивющая надежность результатов и пригодная для целей определения качества спирта этилового.
Библиографическая ссылка
Свечкарь В.П., Буданова Н.А, Григорьева И.В., Пирогова И.М. ИСПОЛЬЗОВАНИЕ ВАЛИДАЦИИ В ФАРМАЦЕВТИЧЕСКОЙ ПРАКТИКЕ НА ПРИМЕРЕ ОПРЕДЕЛЕНИЯ ПРИМЕСЕЙ В СПИРТЕ ЭТИЛОВОМ // Международный журнал прикладных и фундаментальных исследований. 2015. № 7-2. С. 263-267;URL: https://applied-research.ru/ru/article/view?id=7006 (дата обращения: 07.04.2026).