Исследование процесса радиолитического превращения фенолов в водных растворах показало наличие двух каналов:
● Окисление фенолов с ОН- радикалами, образующихся при радиолизе воды;
● Конденсация ароматических ядер с образованием полимерных продуктов а также смол, образующихся в реакциях формальдегида с фенолами [2, 4, 7, 8].
Применялась Фурье-ИК-спектроскопия для исследования твердых остатков. При глубоком каталитическом окислении фенола обнаружено образование нерастворимых полимерных продуктов [8], при окислительном процессе фенола получены ИК-спектры твердых остатков[7], при электроокислении фенола получены ИК-спектры пленок [4], которые совпадают с ИК-спектрами твердых остатков, обнаруженных в работе [7]. В ИК-спектре осадка после окисления фенола в электрохимическом процессе наблюдается интенсивная полоса поглощения в области 3350 см-1, указывающая на образование межмолекулярных водородных связей [7].
При исследовании процесса глубокого каталитического окисления фенола рядом промежуточных соединений о-, п–бензохиноны, о-, п-гидрохиноны, р-гидроксибензойная кислота, тетрогидро-р-бензохинон, малеиновая, малоновая, фумаровая, янтарная, уксусная, щавелевая, глиоксалевая, муравьиная кислот образуются нерастворимые полимерные продукты [8].
В работе [1] установлено повышение интенсивности пиков в области λ = 275 нм, что объясняется с образованием полимерных структур при радиолизе водных растворов резорцина, количество которых увеличивается до дозы 2 кГр, затем с ростом дозы уменьщается.
Несмотря на подробную информацию о продуктах окисления, твердые остатки, образующихся при радиолизе фенолов в водных растворов мало изучены.
Целью работы является изучение твердых остатков, образующихся при радиолизе водных растворов фенола, резорцина и гидрохинона.
Материалы и методы исследования
1,1 г резорцин и гидрохинон, 0,94 г фенол добавляется в воду, объем который составляет 1 л, приготавливаются растворы с концентрацией 0,01 М. Насыщенный воздухом раствор фенола, резорцина и гидрохинона облучали γ-излучением от изотопа 60Со, в статических условиях в стеклянных ампулах при комнатной температуре. Мощность поглощенной дозы составляла 0,21-0,26 Гр/с.
Исследовали твердый осадок, полученный при радиолизе водных растворов фенола и его двухатомных производных. Для анализа взяты твердые осадки, образующихся при радиолизе водного раствора фенола (100 и 200 кГр), резорцина (4 кГр) и гидрохинона (82 кГр). Максимальное количество продуктов образуются при дозе 200 кГр для фенола. Сначала образцы высушивали при комнатной температуре. Снимались Фурье ИК-спектры высушенных остатков после 2 суток.



a б в
Рис. 1.Фотографии твердых осадков полученные при радиолизе водного раствора резорцина при 4 кГр (а); гидрохинона (82 кГр) (б); фенола (200 кГр)(в)
Снимались спектры образцов в виде тонких пленок в ИК-Фурье-спектрометре фирмы Varian 640 FT-IR. С этой целью использовали подложки KBr. Спектры снимались в диапазоне длины волн 4000–400 см-1.
Радиационно-химическое разложение фенола происходит по ступенчатому механизму: на первой стадьи образуются двухатомные фенолы (гидрохинон, резорцин, пирокатехин), далее о-,р- хиноны. После этого разрушается ароматическое кольцо с образованием ди- и монокарбоновых кислот. Фенолы могут взаимодействовать с продуктами, такими как альдегиды, образуя смолаобразные осадки.
Резорцин отличается от фенола повышенной реакционной способностью и может реагировать с формальдегидом без катализаторов и на холоду. Из трех изомерных одноядерных двухатомных фенолов (о-, м- и n-диоксибензолов) только м-диоксибензол (резорцин) способен образовывать пространственные полимеры при поликонденсации с формальдегидом. о-Диоксибензол (пирокатехин) и п-диоксибензол (гидрохинон) образуют олигомеры, которые могут медленно переходить в неплавкое, нерастворимое состояние только при высоких температурах. Это объясняется тем, что второй фенольный гидроксил активирует водород в м-положениях о- и п-диоксибензолов и делает возможным присоединение формальдегида в жестких условиях. В молекуле резорцина вторая гидроксильная группа в значительной степени активирует водород в орто- и пара-положениях. Кроме того, благодаря наличию второго гидроксила становится возможным образование кислородных эфирных мостиков между бензольными ядрами. Поэтому резорцин гораздо более энергично, чем фенол, взаимодействует с формальдегидом, и реакция поликонденсации может протекать без катализатора даже при комнатной температуре. Реакция резорцина с формальдегидом протекает настолько энергично, что полимеры можно получать непосредственно на стадии изготовления изделий [2].
Результаты исследования и их обсуждение
Анализировали твердый осадок методом ИК-спектроскопии. Предполагается что, в системе возникает реакции поликонденсации и образование твердых осадков фенол-формальдегидной смолы (рис. 2), резорцин-формальдегидной смолы, олигомеры гидрохинона [7].
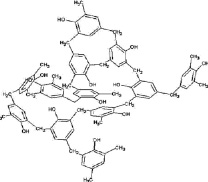
Рис. 2.Структура фенол-формальдегидной смолы
На рис. 3 представлены ИК-спектры твердых осадков полученные при радиолизе водных растворов фенола (10-2М) при поглошенных дозах 100 и 200 КГр.
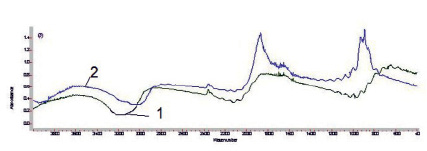
Рис. 3. ИК-спектры твердых осадков, полученные при радиолизе водных растворов фенолов (10-2М) при поглошенами дозами 100 (1) и 200 кГр (2)
Согласно литературным данным [5]:
3700-3300 см-1 – Внутри и межмолекулярные Н связи в димерах и полимерах;
3200-2800 см-1 – Слабые (средние) валентные колебания С-Н связей в ароматических соединениях;
2800-2200 см-1 – Валентные колебания гидроксильной группы;
2100-1700 см-1 – Валентные колебании группы C=O в альдегидах и карбоновых кислотах; предельные алифатические кислоты с группой -CH2-COOH (малоновой кислоты и уксусной),α,β- непредельные кислоты с группой C=C-COOH (муконовой, малеиновой, фумаровой кислоты);
***В области 2000–1600 см-1 все ароматические соединения имеют группу слабых полос (обертона и составные частоты), число и положение которых определяются типом замещания бензольного кольца.
***Пики в областе1700–1634 см-1 соответствует колебаниям 6-цленный цикл и 2 группы С=О в разных циклах в хинонов;
1608-1400 см-1 – Валентные колебания ароматического кольца в аренах и кислоты с Н- связами (муравиная кислота);
1295-1005 см-1 – Плоскостные деформационные колебания С-Н связей 1,2-, 1,4-, 1,2,4-замещенных;
1000-630 см-1 – Внеплокостные деформоционные колебания С-Н связей в аренах, колебания гидроксильной группы и С-О связей в карбоновых кислотах.
Из за неупорядоченной структуры (рис. 2) твердого осадка определить какого рода замещения в бензольном кольце не представляется возможным.
В работе [7] 1600–1500 см-1 показывает валентные колебания ароматического кольца,1440–1300 см-1 деформационная колебания ОН- групов,1620 см-1 группу С=О.
Из сравнении ИК-спектров твердых осадков полученные при радиолизе водных растворов фенолов (10-2М) с поглошенной дозы 100 и 200 кГр видно что, число продуктов больше при высоких дозах (200 кГр).
На рис. 4 представлен ИК-спектр твердых осадков полученный при радиолизе водного раствора гидрохинона (10-2М) при поглошенной дозе 82 кГр.
3800-3200 см-1 – Внутри и межмолекулярные Н связи в димерах и полимерах ;
3100-2600 см-1 – Слабые (средние) валентные колебания С-Н связей в ароматических соединениях;
2400-2000 см-1 – Связанная группа ОН- перекрыванной с валентными колебаниями С-Н в карбоновых кислот;
2100-1700 см-1 – Валентные колебании группы C=O в альдегидах и карбоновых кислотах; предельные алифатические кислоты с группой -CH2-COOH (малоновой кислоты и уксусной), α, β- непредельные кислоты с группой C=C-COOH (муконовой, малеиновой, фумаровой кислоты);
1650-1632 см-1 – Колебании 6-цленный цикл и 2 группы С=О в разных циклах в хинонов и кислоты с Н- связами (муравиная кислота);
1600-1400 см-1 – Валентные колебания ароматического кольца в аренах;
1300-900 см-1 – Внеплокостные дефармоционные колебания С-Н связей в аренах, колебания гидроксильной группы и С-О связей в карбоновых кислотах;
800-550 см-1 – Внеплокостные дефармоционные колебания С-Н в аренах, колебания гидроксильной группы и С-О связей в карбоновых кислотах.
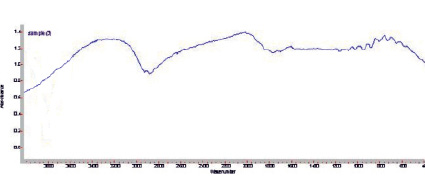
Рис. 4. ИК-спектры твердых осадков полученные при радиолизе водного раствора гидрохинона (10-2М) при поглошенной дозой 82 кГр
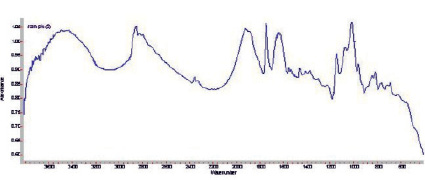
Рис. 5. ИК-спектры твердых осадков полученные при радиолизе водного раствора резорцина (10-2М) при поглошенной дозой 4 кГр
Для кристаллических гидрохинона в нулевом приближении получено менее точное по сравнению с резорцином совпадение расчетных и экспериментальных величин. Это связано с перераспределением электронной плотности внутри молекулы диоксибензолов в зависимости от взаимного положения ОН-заместителей, что и определяет иные динамические и кинематические взаимодействия [6].
На рис. 5 представлен ИК-спектр твердых осадков полученные при радиолизе водного раствора резорцина (10-2М) при поглошенной дозе 4 кГр.
Из ИК-спектра резорцина можно сказать:
3700-3200 см-1 – Внутри и межмолекулярные Н связи в димерах и полимерах;
3100-2500 см-1 – Слабые (средние) валентные колебания С-Н связей в ароматических соединениях;
2400-2000 см-1 – Связанная группа ОН- перекрыванный с валентными колебаниями С-Н в карбоновых кислотах;
2000-1620 см-1 – Образование 1,4-хинона, Валентные колебании группы C=O в альдегидах и карбоновых кислот предельные алифатические кислоты с группой -CH2-COOH (малоновой кислоты и уксусной),α, β- непредельные кислоты с группой C=C-COOH (муконовой, малеиновой, фумаровой кислоты);
1600-1400 см-1 – Предельные алифатические кислоты с группой -CH2-COOH (малоновой кислоты и уксусной), α,β- непредельные кислоты с группой C=C-COOH (муконовой, малеиновой, фумаровой кислоты);
1300-1000 см-1 – Внеплокостные деформоционные колебания С-Н в аренах, колебания гидроксильной группы и С-О связей в карбоновых кислотах;
900-550 см-1 – Внеплокостные деформоционные колебания С-Н в аренах, колебания гидроксильной группы и С-О связей в карбоновых кислотах.
Наблюдаемые нами полосы поглощения совпадает с результатами работы авторов [3], где изучены смолаобразные продукты реакции фенола, резорцина и фенол-резорцина с формальдегидом.
В таблице представлены значения частот ИК-спектров осадков.
Значения частот ИК-спектров осадков
|
Значения частот ИК-спектров осадка,полученного в радиолитическом окислении фенола |
Значения частот ИК-спектров осадка,полученного в радиолитическом окислении резорцина |
Значения частот ИК-спектров осадка,полученного в радиолитическом окислении гидрохинона |
Значения частот ИК-спектров осадка,полученного в электрохимическом окислении фенола [2]. |
Значения частот ИК-спектров пленок, полученных при электроокислении фенола [3]. |
|
Частота, см-1 |
||||
|
668 сл |
624 сл |
571 сл 635 сл |
600 ср |
615 сл |
|
719 сл. |
711 ср. |
700 сл |
– |
|
|
800 ср.шир |
768 ср.шир |
776 ср.шир. |
760 оч.с |
754 оч.с. |
|
848 плечо |
819 плечо |
859 ср.шир. |
820 ср |
830 шир |
|
862 плечо |
844 плечо |
924 плечо |
850 ср.шир. |
830 ср.шир |
|
940 плечо |
961 ср.шир |
– |
980 сл |
971 ср |
|
1075 ср |
1075 ср.шир |
1071 ср |
1070 сл |
1080 сл |
|
1000 ср |
1018 с |
1001 ср |
1090 ср |
1101 ср |
|
– |
1146 шир |
1152 сл |
- |
1152 ср.шир |
|
– |
1227 сл |
1214 сл |
1190 оч.сл |
1212 оч.с. |
|
– |
– |
- |
1235 плечо |
1265 ср |
|
1290 сл |
– |
1320 сл |
1300 плечо |
1288 ср |
|
– |
1452 ср |
– |
1440 ср.шир |
1448 ср.шир. |
|
– |
1463 ср |
– |
1490 с |
1488 с. |
|
– |
– |
– |
1520 ср. |
1504 |
|
1634 сл |
1632 с |
1623 ср. шир. |
1620 ср.шир. |
1610 ср |
|
1652 ср |
1650 с 1682 плечо 1746 с 1920 с |
1648 ср |
1648 ср.шир |
|
|
2362 плечо 2342 плечо 2872 ср.шир 3566 с |
2857 с. 3357 с. |
2033 ср. шир. 2659 ср. шир. 3291 ср. шир. 3415 с |
3350 ср.шир. |
|
|
оч.с.-очень сильный; ср.-срелний; сл.-слабый; шир.-широкий |
||||
В эксперименте в области 1220–1380 см-1 для кристаллического резорцина наблюдается усложнение спектра по сравнению с газобразным состоянием, что можно объяснить формированием у молекулы резорцина в первом случае сильных межмолекулярных водородных связей [6], что наблюдается и в нашей работе.
Спектры резорцина и гидрохинона различаются друг от друга и это можем объяснить с изменением взаимного положения гидроксильных групп, а также влиянием водородных связей.
Выводы
1. Проведенный сравнительный анализ Фурье- ИК спектров фенола и двухатомных фенолов (резорцин, гидрохинон) показывает идентичность колебании группового характера, при этом наблюдаются полосы поглощения в области 3566 см-1(фенол), 3357 см-1 (резорцин), 3415 см-1 (гидрохинон) свидетельствующей о наличии сильных внутри и межмолекулярных водородных связей, характерны для полимерной структуры.
2. С повышением поглощенной дозы от 100 до 200 кГр число продуктов разложения растут, что и подтверждается увеличением интенсивностей полос поглощения. Так как в Фурье-ИК спектрах фенола в области 2100-1700 см-1 (для 200 кГр), в гидрохинона в областях 2400-2000 см-1 и 1300-900 см-1, в резорцине в областях 3100-2500 см-1, 2000-1620 см-1 и 900-550 см-1 наблюдается максимум интенсивностей полос.
Библиографическая ссылка
Кулиева У.А., Курбанов М.А., Гаджиевa Н.Н., Меликова С.З. ФУРЬЕ ИК-СПЕКТРОСКОПИЧЕСКОЕ ИССЛЕДОВАНИЕ ТВЕРДОГО ОСАДКА РАДИАЦИОННО-ХИМИЧЕСКОГО ПРЕВРАЩЕНИЯ ФЕНОЛОВ В ВОДНЫХ РАСТВОРАХ // Международный журнал прикладных и фундаментальных исследований. 2015. № 12-2. С. 247-252;URL: https://applied-research.ru/ru/article/view?id=7895 (дата обращения: 14.05.2026).

