Амилоидоз – это аутовоспалительное системное заболевание, встречающееся у животных и человека. Он характеризуется патологическим синтезом фибриллярного белка в клетках ретикулоэндотелиальной системы с последующим образованием амилоида. Амилоид состоит на 95 % из фибриллярного белка и на 5 % из гликопротеинового Р-компонента. Он способен накапливать в себе конго красный, что используется для прижизненной диагностики амилоидоза [5, 15]. Амилоид стоек к действию различных веществ, однороден, окрашивается эозином в красный цвет, дает реакцию метахромазии при использовании генцианвиолета, метилвиолета, йодгрюна и других красителей [8].
Аутовоспалительными заболеваниями называют гетерогенную группу редких генетически детерминированных состояний, характеризующихся непровоцируемыми приступами воспаления и манифестирующей лихорадкой. Клинические симптомы напоминают ревматические, но при этом отсутствуют аутоиммунные или инфекционные причины. В основе аутовоспалительных заболеваний лежит нарушение функционирования естественного иммунитета, а главным медиатором служит интерлейкин-1 [18]. В отличие от аутоиммунных заболеваний в инициации аутовоспалительных болезней не участвуют механизмы, связанные с синтезом антител или активацией Т-лимфоцитов [11]. У шарпеев амилоидоз является генетическим заболеванием и наследуется по аутосомно-рецессивному пути. Одной из причин возникновения амилоидоза у шарпеев является наследственная лихорадка шарпея (НЛШ). НЛШ – воспалительное заболевание, присущее этой породе [21]. Основной генетический дефект заключается в нарушении восприятия источников воспаления, что приводит к постоянному повышению уровня этих медиаторов в крови. Этот периодический лихорадочный синдром характеризуется сильным повышением температуры, иногда сопровождаемый отеком. Данное заболевание стимулирует синтез в печени белков острой фазы и выброс их в организм. Эти выводы были сделаны на основе биохимического анализа крови шарпея, сделанного во время приступа лихорадки или сразу после его окончания [19].
Вполне возможно, что у НЛШ есть различная возрастная предрасположенность и уровень тяжести течения болезни с точки зрения воспаления, которое он вызывает. У разных особей это может привести к различной степени развития амилоидоза. Например, ответ печени на НЛШ и синтез белков острой фазы, особенно SAA, может быть более острым у некоторых собак, что приводит к более быстрому откладыванию амилоида. У других особей ответ на НЛШ может быть более хроническим, в результате чего амилоид откладывается не так быстро. Точный механизм отложения амилоида может быть различным у разных особей. Например, известно, что шарпеи более восприимчивы к диссеминированному внутрисосудистому свертыванию во время НЛШ, и тромбы в почках могут нанести больше ущерба, чем откладывание амилоида само по себе. У некоторых собак могут быть другие заболевания, которые дополняют эффект амилоидоза.
Стоит иметь в виду, что начальные механизмы отложения амилоида – это нормальный защитный ответ у многих пород собак. У шарпеев же механизм, регулирующий воспалительный ответ, не работает должным образом, позволяя нормальному ответу выйти из под контроля и вызвать заболевание [19].
У шарпеев отложения амилоида могут встречаться в почках, печени, селезенке, поджелудочной железе, надпочечниках, щитовидной железе, миокарде, простате, лимфоузлах и пищеварительном тракте. Чаще всего первыми выходят из строя почки – развивается почечный амилоидоз. Это происходит из-за их низкой регенерации. Амилоид откладывается вокруг клеток, из-за чего происходит их сдавливание, и клетки перестают нормально функционировать. Почки не могут восстанавливаться путем роста новых клеток, поэтому, если клетки погибают, они не заменяются новыми, а структуры, которые они образуют, заменяются фиброзными рубцовыми тканями. Вот почему амилоидный белок в первую очередь вызывает почечную недостаточность. Может присутствовать нефротический синдром, характеризуемый выраженной протеинурией, гипоальбуминемией, гиперхолестеринемией и отеком [22]. Реже встречается печеночная недостаточность от амилоидоза. В отдельных случаях (10-15 %), особенно при генерализованной форме амилоидоза (этиология: тяжелая форма воспаления – серозно-геморрагические, гнойные, гнойно-геморрагические эндоинтоксикации) – при недостаточности почек, печени, заболеваниях желудочно-кишечного тракта; нарушения крово- и лимфообращения) отмечается тяжелый амилоидоз поджелудочной железы, характеризующийся тотальным поражением сосудистого русла железы с образованием тканевых муфт и возможным распространением дистрофического процесса на ткань поджелудочной железы. Особенностью амилоидоза поджелудочной железы является трудность прижизненной диагностики. Это объясняется не только малой информативностью отдельных диагностических приемов (УЗИ, рентгенология), но и особенностью топографической анатомии поджелудочной железы у собак [4, 12].
Почечный амилоидоз, по оценкам, встречается у 23 % шарпеев в США. Истинная его распространенность неизвестна [22].
Возраст появления клинических симптомов типично от 1-6 лет до 9 (в среднем, 4,1 года). Самцы болеют чаще самок (соотношение самки:самцы, 2,5:1). До 23 % шарпеев болеют наследственной лихорадкой шарпеев, которая является причиной развития системного реактивного амилоидоза у этой породы. Наследственная лихорадка шарпеев была обнаружена у 44 % собак. Иногда клинические симптомы амилоидоза проявляются не сразу, и тогда у многих шарпеев наблюдается лихорадка и отечность скакательных суставов, что также является симптомами НЛШ [22].
Амилоидные скопления представляют собой белковые волокна, которые формируются в результате полимеризации частей белка и образуют специфические складчатые тканевые образования, таким образом, обеспечивая амилоид способностью окрашиваться в конго красный и обеспечивая его видимыми свойствами. Благодаря этим свойствам амилоидные структуры являются нерастворимыми и внешне выглядят как воск. При амилоидозе в ткань откладывается аномальный сложный гликопротеид, основой которого являются синтезируемые фибриллярные белки, а к ним добавляются плазменные компоненты в виде глобулиновых белков, фибрина, иммунных комплексов, полисахаридов, мукополисахаридов тканей. Обычно клетки системы мононуклеарных фагоцитов инактивируют этот белок, но при снижении их активности или при гиперпродукции аномального белка происходит его отложение в ткани [10].
Амилоидоз не является специфической болезнью шарпеев, встречается и у человека. В отличие от человеческой формы, у шарпеев он носит реактивную форму. Реактивный амилоидоз – это форма системного амилоидоза, обычно возникающего на фоне хронических воспалительных заболеваний и характеризующегося отложением амилоидного белка АА. Амилоидный белок АА является производной формой белка острой фазы, а именно – амилоидного белка А сыворотки крови, вырабатываемого печенью. Важно понимать, что амилоидный протеин АА – это нормальный белок, и что его выработка печенью – это нормальная реакция на повреждение тканей и воспаление [19]. Также амилоидоз у собак связан с бластомикозом, системной красной волчанкой, циклической нейтропенией, печеночной гемангиомой и различными воспалительными заболеваниями. В науке известны случаи у собак без очевидных воспалительных или новообразовательных процессов [16].
У собак АА амилоидоз встречается обычно после 9-10 лет [17], носит генерализованный характер, но клинически проявляется поражением почек [15, 18]. У шарпеев он развивается в возрасте 1-4 лет [1, 16].
Смерть от амилоидоза отмечена у щенков не моложе 8 месяцев и не старше 12 лет. Чаще всего умирают в возрасте 3-5 лет.
Патогенез. Белок амилоид А, сформированный путем полимеризации конечной части аминокислот сывороточного амилоида А (SAA – альфа-глобулин) в ответ на воспалительные цитокины, является первичным протеином, вовлеченным в процесс реактивного амилоидоза. Уровень SAA очень сильно увеличивается за счет синтеза печенью при неоплазии, хронической инфекции, воспалении [1].
Больные шарпеи имеют увеличенную концентрацию интерлейкина-6, цитокина, который стимулирует синтез SAA и выпуск его из гепатоцитов. Другие цитокины (например, опухолевой фактор -α, интерлейкин-1β) также вовлекаются в этот процесс. Эти цитокины вызывают ответ острой фазы, который характеризуется лихорадкой, продукцией печенью белков острой фазы (включая SAA) и мобилизацией нейтрофилов.
Механизм развития амилоидоза почек подчинен закономерностям развития АА-амилоидоза, при котором фибриллы амилоида образуются из поступающего в макрофаг – амилоидобласт плазменного предшественника фибриллярного белка амилоида – белка SAA, который усиленно синтезируется в печени под влиянием макрофагального медиатора интерлейкина-1, что приводит к резкому увеличению содержания SAA в крови [6].
Симптомы. Чаще всего при почечном амилоидозе у собак отмечаются следующие симптомы: анорексия, полиурия и полидипсия, слабость, вялость, рвота, обезвоживание, потеря веса. У шарепеев они аналогичны, что указывает на хроническую почечную недостаточность. Гематологические исследования у собак с амилоидозом включают лейкоцитоз и нерегенеративную анемию. Наблюдается азотемия, гиперфосфатемия, метаболический ацидоз, гиперхолестеролемия, гипопротеинемия. [16]
Амилоидоз почек у других пород собак может вести к выраженной протеинурии. Только 25-43 % больных шарпеев имеют протеинурию [22]. Следует отметить, что у шарпеев наблюдается медуллярный амилоидоз без вовлечения гломерул, в отличие от других пород собак [3].
Как уже было отмечено, при откладывании амилоида чаще всего страдают почки, но также его можно обнаружить в селезенке, печени, надпочечниках, поджелудочной и щитовидной железах, сердце, подслизистой оболочке кишечника. Амилоидоз печени часто проявляется желтухой [16].
Некоторые больные собаки имеют увеличенный риск тромбоэмболического заболевания, частично из-за потери антитромбина через поврежденные гломерулы. Тромбоэмболия встречается у 40 % собак с амилоидозом [13].
Диагноз. Одним из лабораторных методов исследования является определение протеинурии и креатининурии. Однако точный диагноз ставится на основании исследования гистологической биопсии печени или почек при окрашивании конго красным. Световая микроскопия показывает отложения амилоида в различных оттенках красного цвета. Поляризующая микроскопия показывает отложения амилоида в виде двойного лучепреломления, похожего на зеленое яблоко. Накопление амилоида подтверждается обесцвечиванием окрашенных конго красным отложений при окислении калия перманганатом [1]. На раннем этапе развития заболевания для обнаружения патологических изменений почек и печени у молодых шарпеев можно использовать ультразвуковое исследование.
Приблизительно у 64 % шарпеев наблюдается поражение гломерулярного аппарата.
Также берут анализ мочи. Протеинурия рассматривается как характерная особенность гломерулярного заболевания, но является вариабельной (25 %-43 %) при лихорадке шарпеев, поскольку отложение амилоида встречается, главным образом, в мозговом слое почек [22].
Патоморфологические изменения. Как уже было отмечено, амилоидоз у шарпеев является системным заболеванием, при котором затрагиваются практически все органы. Однако больше всего страдают печень и почки. Это же заметно при патанатомическом исследовании павших животных.
При амилоидозе печени амилоид откладывается сначала в межбалочном пространстве, что ведет к нарушению балочного строения и атрофии печеночных клеток. Далее их место занимает фибриллярный белок, который полностью замещает гепатоциты в печеночной дольке. На рис. 1 (окраска гематоксилин-эозин, увеличение 200) хорошо заметно мощное отложение амилоида в печеночной дольке, начинающееся с межбалочного пространства и ведущее к атрофии гепатоцитов. Макроскопически это проявляется увеличением печени в объеме, приобретением ею гомогенной структуры без сохранения рисунка ткани [8].
При амилоидозе почек в начальной стадии процесса амилоид откладывается в клубочках, затем – в собственной оболочке канальцев, а при резко выраженной форме – между канальцами в межуточной соединительной ткани. Исследуя препарат, можно заметить атрофические изменения в канальцах, клубочках, что заканчивается их распадом. При слабом увеличении в ранних процессах в клубочках можно различить сосудистое сплетение, ядра эндотелия, форменные элементы в просвете сосудов. Амилоид обнаруживается между сосудистыми петлями клубочка в виде небольших гомогенных глыбок, слабо окрашенных эозином. В сильно выраженных случаях фибриллярный белок полностью заполняет клубочек, просветы сосудов сдавливаются, становятся неразличимы, клетки эндотелия атрофируются, их количество уменьшается. На высшей стадии процесса клубочки находят гомогенными и бедными ядрами. Среди глыб или сплошных масс амилоида встречаются лишь единичные сохранившиеся ядра эндотелия. При отложении амилоида в капсуле клубочков она становится толстой, а структура ее может сливаться с пораженным клубочком. При отложении амилоида в собственную оболочку канальцев она резко утолщается, имеет вид гомогенных колец или муфт, окружающих канальцы (рис. 2) [7].
При длительном процессе отложение аномального белка заметно и в селезенке. В начале процесса, т.е при очаговой форме, амилоид откладывается в фолликулах белой пульпы. Это приводит к резкому увеличению фолликулов в объеме и атрофии красной пульпы от давления. В дальнейшем происходит отложение амилоида и в красную пульпу. Процесс приобретает диффузный характер. В исходе имеем гомогенное отложение амилоида с полной атрофией клеточных элементов. Лишь кое-где клетки паренхимы селезенки остаются в виде разрозненных, плохо просматриваемых участков (рис. 3, рис. 4) [7].
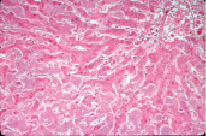
Рис. 1. Амилоидоз печени. Микрокартина. Окраска гематоксилин-эозин. Увеличение 200
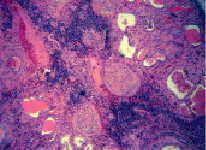
Рис. 2. Амилоидоз почки. Микрокартина. Окраска гематоксилин-эозин. Увеличение 200

Рис. 3. Амилоидоз селезенки. Саговая форма. Микрокартина. Окраска гематоксилин-эозин. Увеличение 200
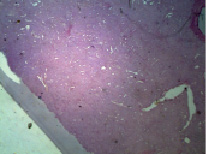
Рис. 4. Амилоидоз селезенки. Сальная форма. Микрокартина. Окраска гематоксилин-эозин. Увеличение 200
Лечение. Прогноз при амилоидозе шарпеев неблагоприятный у большинства собак, за исключением случаев, когда первопричина была вовремя обнаружена и устранена. Лечение должно быть направлено на устранение этиологического фактора. Нужно помнить, что оно будет эффективным только на первой стадии заболевания. Также следует помнить о симптоматической и поддерживающей терапии. Питание должно быть хорошего качества, а при развитии амилоидоза – с низким содержанием жиров и белка. В рацион следует вводить биодобавки, содержащие полиненасыщенные жирные кислоты Омега 3, которые оказывают антиоксидантное и противовоспалительное действие.
У человека для предотвращения амилоидоза используется колхицин как специфическое средство. Также его стали использовать и у животных. Он блокирует синтез и секрецию белка SAA в печени, таким образом предотвращая продукцию амилоид усиливающего фактора и откладывание амилоида. В процессе отложения амилоида в органах различают несколько фаз. В зависимости от фазы колхицин может быть эффективен только на ранних этапах заболевания, и при появлении почечной недостаточности теряет свою эффективность. В преднакопительную фазу концентрация сывороточного амилоида А становится высокой, но пока без отложения амилоида. Включение в лечение колхицина может предотвратить развитие данной болезни. В фазу накопления содержание амилоида быстро увеличивается. Включение колхицина замедляет, но не предотвращает отложение амилоида. В фазу накопления (стадия плато) смещение накопления амилоида варьируется незначительно. Никакие препараты не дают каких-либо результатов.
Колхицин относится к средствам, влияющим на обмен мочевой кислоты. Также известен как противоподагрический препарат, обладает противовоспалительным эффектом. Характеризуется как алкалоид клубнелуковиц безвременника великолепного семейства лилейных. Белый или белый с желтоватым оттенком мелкокристаллический порошок, темнеющий на свету. Колхицин подавляет митотическую активность гранулоцитов за счет взаимодействия с их микротубулярным белком. Угнетает миграцию гранулоцитов в очаг воспаления, уменьшает продукцию гликопротеина, молочной кислоты и ферментов, возникающую во время фагоцитоза гранулоцитами кристаллов мочевой кислоты [14]. Уменьшает утилизацию глюкозы фагоцитирующими и нефагоцитирующими лейкоцитами, препятствует образованию амилоидных фибрилл. Нарушает нейромышечную передачу, стимулирует функции желудочно-кишечного тракта, угнетает дыхательный центр, суживает сосуды и повышает артериальное давление, понижает температуру тела [2]. Также колхицин повышает активность коллагеназы, является мощным ингибитором клеточного митоза. Он эффективен при аутовоспалительных заболеваниях, так как блокирует выработку интерлейкина-1. Способен тормозить периодические изменения в моноцитарной и нейтрофильной активации к эндотоксину, связанные с эпизодической природой НЛШ [20].
Колхицин следует с осторожностью применять старым или истощенным животным. При беременности его следует использовать только если польза от него будет больше, чем вред. Колхицин может вызывать у собак тошноту, рвоту и диарею. Также может появиться боль в животе, наблюдается снижение аппетита. Не рекомендуется применять колхицин совместно с нестероидными противовоспалительными препаратами и другими препаратами, вызывающими миелодепрессию, так как они повышают риск лейкопении и тромбоцитопении [6].
При появлении побочных эффектов после применения колхицина, дачу препарата следует прекратить на несколько дней, а затем возобновить терапию, используя дозу раз в день или давать по половине дозы дважды в день. Когда собака привыкнет к препарату, можно начинать давать ей колхицин в полной дозировке. J. Vidt в своей статье рекомендует давать шарпеям с НЛШ 0,6 мг (1 таблетку) препарата дважды в день. Также колхицин можно использовать для профилактики амилоидоза [19].
Побочные эффекты колхицина включают рвоту и диарею. При длительном назначении наблюдаются супрессия костного мозга (апластическая анемия, агранулоцитоз, лейкопения, тромбоцитопения) и гипертензия. Отмечаются печеночная недостаточность и нарушение функции почек, миопатия, повышение уровня щелочной фосфатазы, синдром мальабсорбции, проявляющийся дефицитом витамина В12. Также могут возникать кожные аллергические реакции, местное раздражение при внутривенном введении препарата в виде резкой болb и некроза в области инъекции [2].
В заключение следует еще раз отметить, что наследственный амилоидоз у шарпеев – системное заболевание, при котором в процесс включаются все органы и системы органов. Клиническая картина проявляется не сразу, и достоверно поставить правильный диагноз бывает очень сложно. При этом следует помнить, что лечение амилоидоза возможно только на ранних этапах развития. Именно поэтому изучение данного заболевания очень важно, что в дальнейшем поможет верно определить проблему и своевременно начать терапию.
Библиографическая ссылка
Паршина В.И., Куликов Е.В., Попова И.А. НАСЛЕДСТВЕННЫЙ АМИЛОИДОЗ У ШАРПЕЕВ // Международный журнал прикладных и фундаментальных исследований. 2016. № 2-4. С. 564-569;URL: https://applied-research.ru/ru/article/view?id=8639 (дата обращения: 22.05.2026).

